2000年代に入り、次世代シーケンサーの登場によって大規模なゲノム解析が可能となり、その結果、腸内細菌をはじめとするヒトに常在する微生物の研究は飛躍的に進歩した。一方、約9000種類ともいわれているヒトに感染するウイルスについては、ほとんど解明されていないのが現状だ。これまでに39種類のウイルスがヒトの体内にいることが明らかになっているが、私たちの体や健康にどう影響するかは未知の部分が多い。今後の研究が期待される。
特集 知られざるウイルス 今後の研究が注目される「ヒト」と「ウイルス」の関係
構成/大内ゆみ
近年、動物や植物などの組織に含まれるすべての核酸(DNA/RNA)を網羅的に解析するメタゲノム解析が進んでいます。ウイルス研究でも、そうしたサンプルに含まれるウイルスを網羅的に同定するバイローム(ウイルス叢)解析が試みられています。その目的の多くは、病原体としてヒトや動物に感染する未知のウイルスを探し出すことです。例えば、原因のわからない発熱があり感染症を疑ったときに、患者の組織からウイルスを検索します。あるいは、野生動物の間で流行している、将来ヒトに感染症を引き起こすかもしれないウイルスを探索したりもします。こうした取り組みを進めている世界的なプロジェクトとして“Global Virome Project”があり、ここではヒトに感染するウイルスの種類の数は、現在定義されている約9000種に対して63万から83万種程度と推計し、まだ発見されていないウイルスが多くあることを示しています。
現在、新型コロナウイルス感染症(COVID-19)も含め、疾患を対象としたバイローム研究が進み、日本ではエゾウイルスなど新たなウイルスも発見されています。感染症は人類にとって脅威となるため、どうしても病原体としてのウイルスがフォーカスされがちですが、実は健常なヒトにもウイルスが存在していることは昔から知られています。
- * エゾウイルス:北海道大学人獣共通感染症国際共同研究所らの研究グループが発見した、マダニが媒介するウイルス。2021 年に発表された。発熱や筋肉痛などを主徴とする感染症の原因とされる。
健常なヒトに39種類のウイルスが存在
例えば、ヘルペスウイルスは自然界に広く存在し、魚類や両生類、哺乳類などの脊椎動物に感染します。ヒトに感染するヘルペスウイルス(ヒトヘルペスウイルス)の一種であるエプスタイン・バール・ウイルス(EBV)は、成人の9割近くが感染しているとされていますが、疲労感や発熱などの症状を引き起こすことはまれです。このように、宿主に感染し増殖していても症状を起こさない感染様式を不顕性感染といいます。
また、生体内に潜入したウイルスが発症の有無にかかわらず、いったん増殖のサイクルを止めて臓器や組織に留まり続け、何らかの理由で免疫機能が低下したときに再活性化する感染様式を潜伏感染といい、前述のヘルペスウイルスのほとんどにその特性があります。
他にも、私たちの体の中にはさまざまなウイルスが不顕性感染もしくは潜伏感染していると考えられ、それがヒトの各組織に何らかの影響を与えている可能性があります。しかし、病気にかかっていないヒトから臓器組織を採取することは難しく、健常なヒトでウイルスがどの臓器に、どの程度の割合で存在しているのかはわかっていませんでした。そこで当研究室では当時大学院生であった熊田隆一氏が中心となり、健常なヒト組織全体を対象としたバイロームの研究を世界で初めて行ったのです。サンプルとして、アメリカの巨大なゲノムプロジェクトの“The Genotype-Tissue Expression (GTEx)project”が提供するRNAシーケンシングデータ(RNAの配列情報)を用いました。もし何らかのウイルスに感染しているとすると、ウイルスのRNAが増殖し、RNAシーケンシングデータの中にもウイルス由来の配列が含まれていることが想定されるからです。
このデータは、アメリカで検視となった遺体から得られたもので、厳密に“健常な”とはいえませんが、少なくとも死因が感染症ではないデータです。もともとこのGTExプロジェクトの目的は、遺伝的多型(個人間における塩基配列の違い)が、各組織における遺伝子発現にどのような影響を与えるかを明らかにするものですが、1000人以上の54種類の組織から採取したRNAシーケンシングデータと臓器組織の顕微鏡標本の画像が公共のデータベースとして公開されています。そのサンプル数は1万以上もあり、情報量は100テラバイトに及ぶいわばビッグデータです。そのため、解析には当研究所のスーパーコンピュータ「SHIROKANE」を用いました。これまでのゲノム研究により蓄積したデータが再利用でき、情報解析の技術が進展した現在だからこそ、実現した研究だといえるかもしれません。
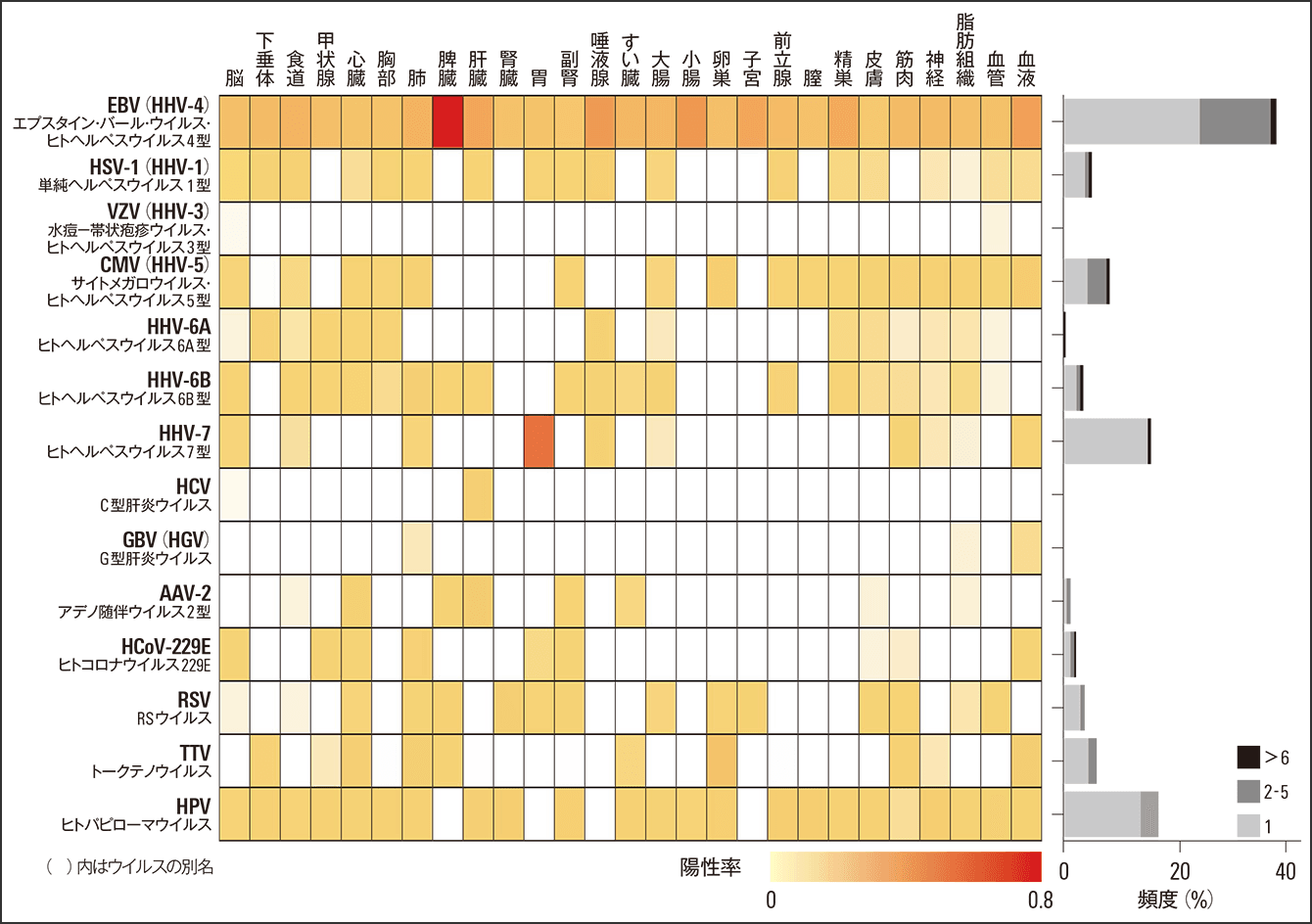
まずは、GTExのデータからアメリカ国立生物工学情報センターに登録されている5139種類のウイルスのゲノム情報をもとにウイルスに由来すると考えられるRNA配列を検索しました。その結果、39種類のウイルスが検出され、各ウイルスの臓器ごとの陽性率(検出された頻度)が明らかになりました(図1)。
 (Kumata R, et al. BMC Biology (2020) 18:55を改変)
(Kumata R, et al. BMC Biology (2020) 18:55を改変)
図1 検出された主なウイルスと部位各ウイルスにおけるヒトの組織ごとの陽性率。色が濃いほど、陽性率が高いことを示す。棒グラフはそれぞれのウイルスが陽性であった個体の頻度。
検出されたウイルスの多くは、ヒトに感染することがよく知られているウイルスです。前述のヒトヘルペスウイルスや季節性の風邪の原因となるヒトコロナウイルスの一種、乳幼児期に感染し気管支炎や肺炎などの原因になるRSウイルス、子宮頸がんの発症に関わるヒトパピローマウイルス、C型肝炎ウイルス(HCV)などです。これは当然といえば当然の結果で、これまでの知見を反映した結果だといえます。しかし中には、健常なヒトからたびたび検出されるものの、病原性などが明らかになっていないウイルスも検出されました。
一方で、ヒト以外の脊椎動物、昆虫、植物などに感染するウイルスも含まれていました。ただし、ヒト以外に感染するウイルスの場合、陽性率が低いため、感染しているわけではなく、たまたま組織にいた可能性が高いと考えられます。
例えば、トマトに感染するウイルス(トマト黄化えそウイルス)が見つかりましたが、そのウイルスに感染したトマトを食べて、胃などの組織にそれが残っていたのかもしれません。
また、組織ごとのウイルスの有無に注目すると、EBVや単純ヘルペスウイルス1型(HSV-1)のように全身、もしくは多くの組織にわたり存在するウイルスもあれば、ある組織に特異的に存在するウイルスもあることがわかりました。
実はこの研究を始める前は、もっと多くのウイルスが高頻度に検出されるのではないかと推測していました。例えば、人獣共通感染症の原因になりうるようなヒト以外の動物に感染するウイルスです。しかし、そうした強い影響力を持つウイルスは検出されず、これは人類にとって良い結果だといえるでしょう。
ヒトの免疫反応や生理的機能への影響
さらにこの研究では、ヒトの遺伝子発現とウイルス由来の遺伝子の有無との関連を解析し、ヒトの体内に存在するウイルスがどのような影響を与えているのかを調べています。その結果、いくつかのウイルスにおいて、ヒトの免疫反応に特徴がみられました(図2)。
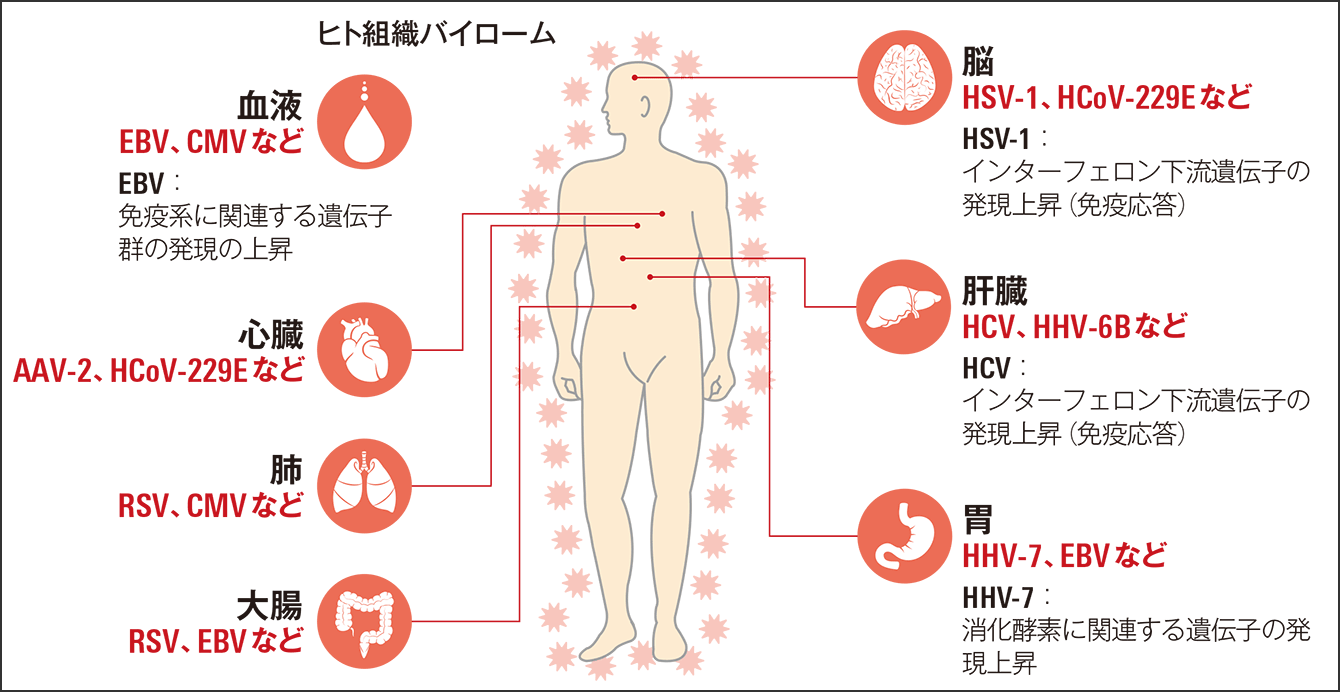
図2 検出された主なウイルスとヒトとの関連性健常人の脳や肺、心臓、消化器官、血液や神経などにはさまざまな種類のウイルスが存在する。その中には臓器特異性や強い免疫反応、臓器の状態と関連する可能性を示すウイルスがある。
その一つがHCVで、肝臓以外の臓器からはほとんど検出されず、臓器特異性がありました。肝臓136検体のうち3検体が陽性であり、これらの検体では、免疫系細胞から分泌されるタンパク質であるインターフェロンによって制御される遺伝子群(下流遺伝子)の発現が顕著に増加していました。インターフェロンはウイルス感染に際して生体内でリンパ球などから産生され、その下流遺伝子の発現は自然免疫反応の強さを測る指標とされています。つまり、HCVが陽性の検体では、強い免疫反応を示していたのです。
また、HCV陽性の検体の顕微鏡標本の画像を病理学の医師に見てもらうと、肝炎症状を呈していることもわかりました。直接的な死因ではなかったとしてもHCVに感染し、肝炎を発症していた可能性が考えられます。
同じく強い免疫反応が示されたウイルスが、HSV-1です。HSV-1は、唇やその周辺に小さな水ぶくれができる口唇ヘルペスの原因ウイルスとして知られていますが、HSV-1が脳に到達すると、脳炎を起こし、死に至ることもあります。ある検体では脳組織からHSV-1のRNAが大量に検出され、インターフェロン下流遺伝子の発現が顕著に増加していました。恐らく、脳炎を発症していたと推測されます。他にもEBV陽性の検体では、EBVが感染する主要な細胞だとされているB細胞を多く含む血液や脾臓で、免疫系に関連する遺伝子群の発現が上昇していました。
以上のようなウイルスは、明らかな病原性がわかっているウイルスです。では、顕著な病原性が知られていないウイルスではどうなのか。例えば、トークテノウイルス(TTV)は病原性が不明で、健常なヒトから検出されることが知られており、今回の研究でも複数の臓器検体から検出されました。TTV陽性と陰性の検体を比較すると、インターフェロン下流遺伝子の発現に差がないことがわかりました。つまり、ヒトの免疫反応を回避しつつ、体内に不顕性感染していることが考えられるのです。この結果だけではわかりませんが、TTVがヒトに何らかの影響を及ぼしている可能性もあります。
さらに免疫反応だけではなく、ヒトの生理的な機能に影響を与えている可能性があるウイルスもみられました。それがヒトヘルペスウイルス7型(HHV-7)で、乳幼児期に感染し突発性発疹を起こすことが知られています。成人のほとんどがHHV-7の抗体を持ち、潜伏感染していることがわかっていますが、成人での病原性は明らかになっていません。
今回の研究でも、血液や脳、肺や筋肉など複数の臓器組織から検出されましたが、中でも胃において高い陽性率が示されました。胃からHHV-7が検出されたのは初めてのことです。
しかも、HHV-7陽性と陰性の胃の検体では、胃における遺伝子の発現パターンが大きく異なっていることもわかりました。さらに、どの遺伝子の発現が異なるのかを調べたところ、陽性が多いグループでは消化酵素に関連する遺伝子の発現が大きく上昇していました。この結果については、以下のことが考察されます。
一つには、HHV-7の感染によって胃における遺伝子パターンが変化した、あるいはその逆でHHV-7が特定の遺伝子の発現パターンを示す胃に感染しやすいのではないか。加えて、このデータでは胃のどこの部分を採取したかは不明であるため、胃の特定部分のみにHHV-7が感染しているという可能性もあります。関連解析のため、因果関係まではわかりませんが、HHV-7感染が胃の状態と関連する可能性があることは確かです。
COVID-19で進歩するバイローム研究
以上のように、この研究ではヒトとウイルスとの共生関係の一端が示されました。本研究で用いた解析手法をさまざまなRNAシーケンシングデータに応用すれば、さらなる展開が可能だと考えています。例えば、今回用いたデータはアメリカ人を対象としたもので、さまざまな人種が含まれていますが、人種、さらには性別でもバイロームは異なると考えられます。データによっては、そうした人種や性別に特化した解析も可能です。
さらに、原因不明の感染症の病原体の特定はもちろん、一見ウイルスと関連のないような病気、例えば糖尿病などの遺伝的多型による発症のリスク情報と、バイロームの情報を合わせることで、疾患のかかりやすさと常在するウイルスとの関連性が明らかになることも期待されます。
そもそもバイローム研究は、近年盛んに行われている細菌叢(マイクロバイオーム)研究と比べ、研究が遅れていました。その一因として、細菌はすべての細菌が共通で持っている遺伝子がいくつかあるのに対して、ウイルスは共通の遺伝子が存在しないことがあります。しかし、この研究の手法を用いれば、多くのウイルスをターゲットとした解析が可能です。
また、マイクロバイオーム研究では、ヒトの皮膚や体内に数百兆個の細菌が存在するといわれています。それに対し、ヒトの皮膚や体内に存在するウイルスの数は380兆個と推測する説がありますが、実はその多くは細菌に感染するウイルス(ファージ)だといわれています。こうしたファージ叢に注目した研究も興味深いテーマでしょう。
現在、COVID-19の世界的流行により、ウイルス学は大きな進歩を遂げています。この研究のように、生命の問題を情報解析によって解く生命情報学の研究者がウイルス学分野に多く流入してきているのです。今後、バイローム研究が発展し、ヒトとウイルスとの共生関係が明らかになると期待しています。