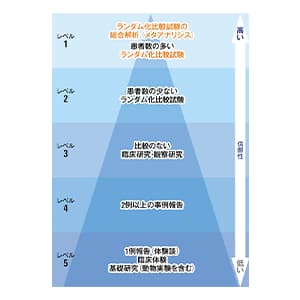
標準治療は長期にわたるがん研究の集積だが、既存の治療法のほとんどが、がん細胞以外の正常細胞にもなんらかの障害を与え副作用を引き起こすという課題を残す。一方、画期的なコンセプトによる効果的な治療法が誕生している。筆頭が、光エネルギーでがん細胞を破壊すると同時に免疫を活性化させ、正常細胞に障害を与えずにがん細胞と免疫抑制細胞だけを選択的に殺す光免疫療法だ。論理は確立されており、一部のがんが保険適用になっている。今後の進展が期待される。
〈シリーズ〉がんから身をまもる
第4回 標準治療と先進医療 がん細胞と免疫抑制細胞を選択的に殺す光免疫療法
構成/飯塚りえ イラストレーション/小湊好治
がん細胞が異常に増えて生命を脅かすという病気が、がんです。これを克服すべく、研究が重ねられ、外科手術、放射線治療、薬物療法といった3大治療によって、多くの患者が命を永らえることができるようになりました。しかし、どの治療においても後遺症や副作用は解決されておらず、転移、再発の不安も残ります。がん治療の決定打とはなっていないのです。
がん細胞と同時に正常細胞も障害
既存のがん治療の課題を改めて見てみます。
最初に、既存の治療法はほぼすべて、がん細胞以外の正常な細胞にも障害を与えます。薬物療法で使われている薬剤は、いずれも毒性の強い化合物です。抗がん剤が全身に行きわたるため、がん細胞を殺すと同時に正常細胞にも障害を与えることとなり、脱毛や倦怠感といった副作用があります。放射線治療の場合では、照射した周辺の正常細胞だけでなく、組織を再生させる幹細胞や免疫細胞にも強いダメージを与えます。治療痕が残ったり、組織の萎縮によって臓器が機能障害を起こしたりすることもあります。こちらも治療の後遺症は深刻な問題です。そして、どちらの療法にも、投与量、照射量に限界があり、がんが残っていてもそれ以上の処置ができなくなります。転移したがんや再発がんには効果が見られないこともあります。私はこれらの課題を克服すべく、がん細胞を選択的に殺し、正常細胞には障害を与えず、使用回数に制限がなく、再発を抑えて、転移がんにも有効な治療法を模索し、たどり着いたのが「光免疫療法」です。
光免疫療法の仕組みはシンプルです(図1)。がん細胞に特異的に結合する抗体分子に、光で反応する特殊な物質を搭載し、腫瘍部分に近赤外光を照射します。すると、光に反応した分子が化学反応を起こし、がん細胞が壊れていくというものです。この療法のメインプレイヤーである、抗体、光、そしてIR700という化合物について、順を追って説明していきましょう。
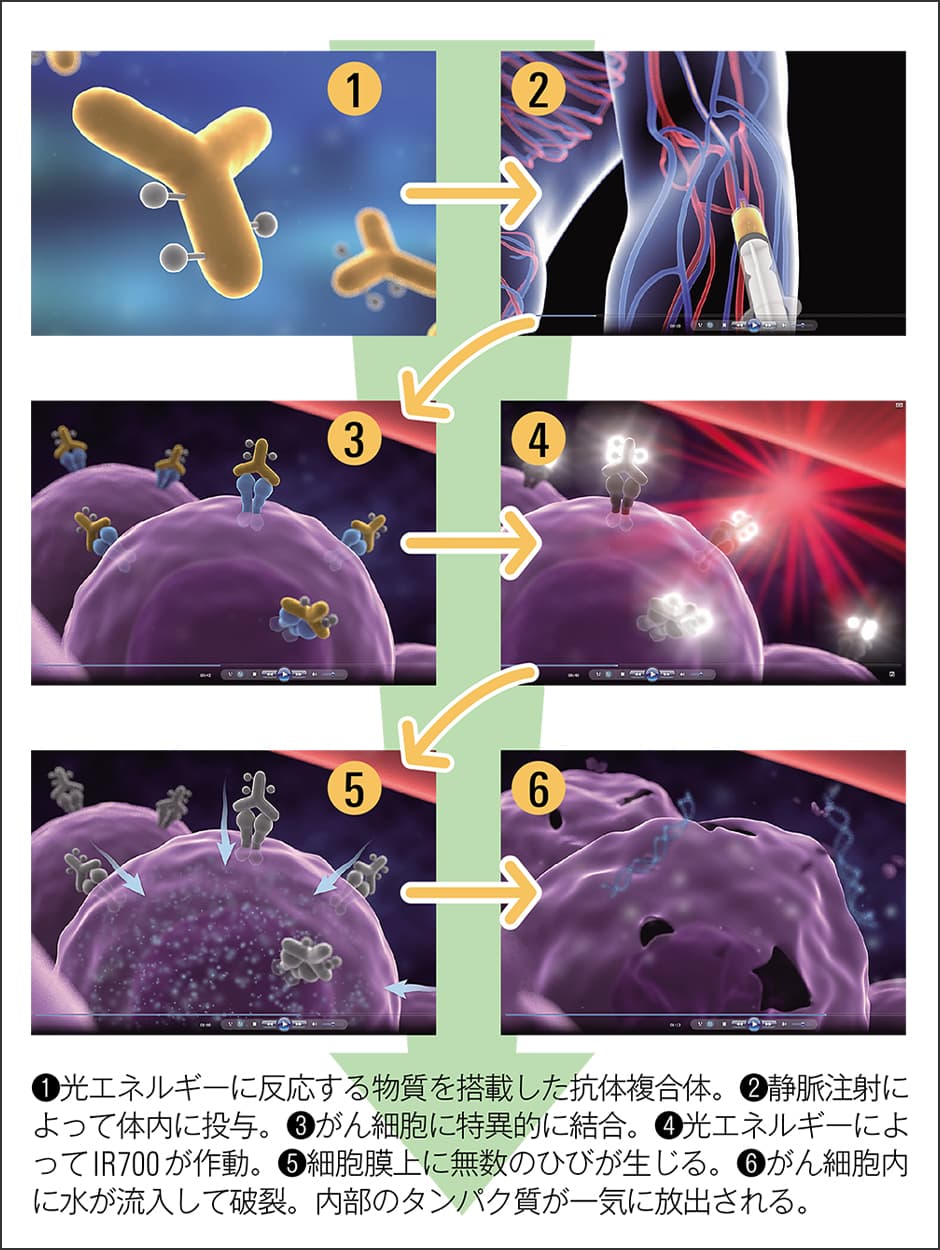
図1 光免疫療法の仕組み
正常細胞に障害を与えず、がん細胞だけを攻撃するためには、細胞を特異的に選択する必要があります。これについては、医学生時代に出合った抗体という分子が、光免疫療法の方向性を決定づけるものとなりました。抗体はそれぞれ、結合するタンパク質(抗原)が決まっており、生物的な分子を選択する特異性において、抗体以上に優れたものは他にありません。体外でも安定していて化学的な修飾がしやすく、現在の医療、医学において抗体分子は欠かせないツールとなっています。病理組織診断では、組織を染色してがんかどうかを判断するために抗体が使われており、体内でがん細胞に特異的に結合する物質として最適なのです。
次に、選択したがん細胞をどのように殺すか、という問題です。
薬と毒は表裏一体であって、全身を巡る“毒”を投与するという方法では、がん細胞以外の場所で薬の毒性が発揮されて正常細胞に害が及ぶ可能性を払拭できません。薬を用いずに細胞を壊す手法を検討するうえで、発想を転換する必要がありました。
光エネルギーでがん細胞を破壊する
生物の細胞は、見方を変えると、遺伝子という設計図によって作られた非常に精巧な機械と考えることができます。そしてこの精密機械を完全に壊す最も有効な方法は、内部の部品をまとめて覆って守る外面、つまり細胞膜を壊してしまうことです。これまでの多くの薬や放射線治療は、細胞中のDNAに障害を与えて死滅させることを目指していましたが、精密機械である細胞にはDNAの傷を修復させたり薬剤耐性を持ったりという精巧な機構があり、簡単に壊すことができません。しかし、細胞膜が壊れてしまったら細胞は絶対に生きていけません。「機械を壊す」には物理的な刺激を与えればよいのです。
がん細胞を破壊する装置のスイッチとして選んだのが光エネルギーです。私は、それ以前にがん細胞のイメージングの研究に携わっていました。体内でがんを選択的に光らせる物質の開発は、同時に体内でがんを選択的に殺すための治療法の開発にもつながると考えてのことでした。光免疫療法では、可視光と赤外線の中間に位置する近赤外光を使います。100〜400nm以下の紫外線より波長の短い光はDNAに損傷を与えてしまいます。また可視光(400〜750nm程度)はよほど強く照射しない限り無害ですが、体内ではヘモグロビンなどに吸収されて体内に到達しません。これらを鑑みると、利用できる光の中では最もエネルギーの高い700nmの近赤外光に絞られました。
開発のごく初期には光の照射範囲が限られていましたが、現在は、光ファイバーを利用して3cm以上の大きながんや、すい臓、肝臓など体内深部のがんに照射が可能です。光ファイバーは直径1㎜ほどですから、がんの塊に細い針付きのチューブを差し込み、針を抜いて代わりに光ファイバーを挿入し内側から照射しています。この手技は、エコーやCTといった装置で体内の断面画像を確認しながら行われており、ほぼ狂いなく針が置かれます。今後、装置もさらに改良されていくと思われます。
次に必要なのは、この光を用いて細胞を破壊するための物質です。そして出合ったのが、IR700(IRDye® 700DX)という化合物でした。
IR700のもとは、フタロシアニンという化合物で、新幹線の車体の塗装にも使われているような顔料に用いられます。強固な不溶性を持つ物質でかつ近赤外光のエネルギーを吸収する性質もあります。この物質を水溶性にする加工を施したものがIR700です。
光免疫療法のプレイヤーの性質を理解してもらったところで、機序を詳しく説明しましょう。
光免疫療法では、高い特異性を持ってがん細胞に結合する抗体にIR700を搭載した複合体を体内に投与します。そして、抗体ががん細胞表面の抗原にくっついた頃(通常投与から1〜2日程度)、近赤外光を照射します。するとIR700は、光エネルギーに反応して水溶性の性質が変化して超不溶性となります。このフタロシアニンは、水の中では単体で存在できず、結合している抗原と抗体が変形したり重合したりしてIR700を水分子から覆い隠すような振る舞いを見せます。するとがんの細胞膜上に小さな傷がつき、その結果、細胞内に水が流入してがん細胞が膨れ上がり、やがて細胞膜が大きく裂けて壊れてしまうのです。あたかも膨れ上がった風船がパチンと壊れるかのように、みるみる細胞が壊れていく様子が顕微鏡で観察できました(図2)。
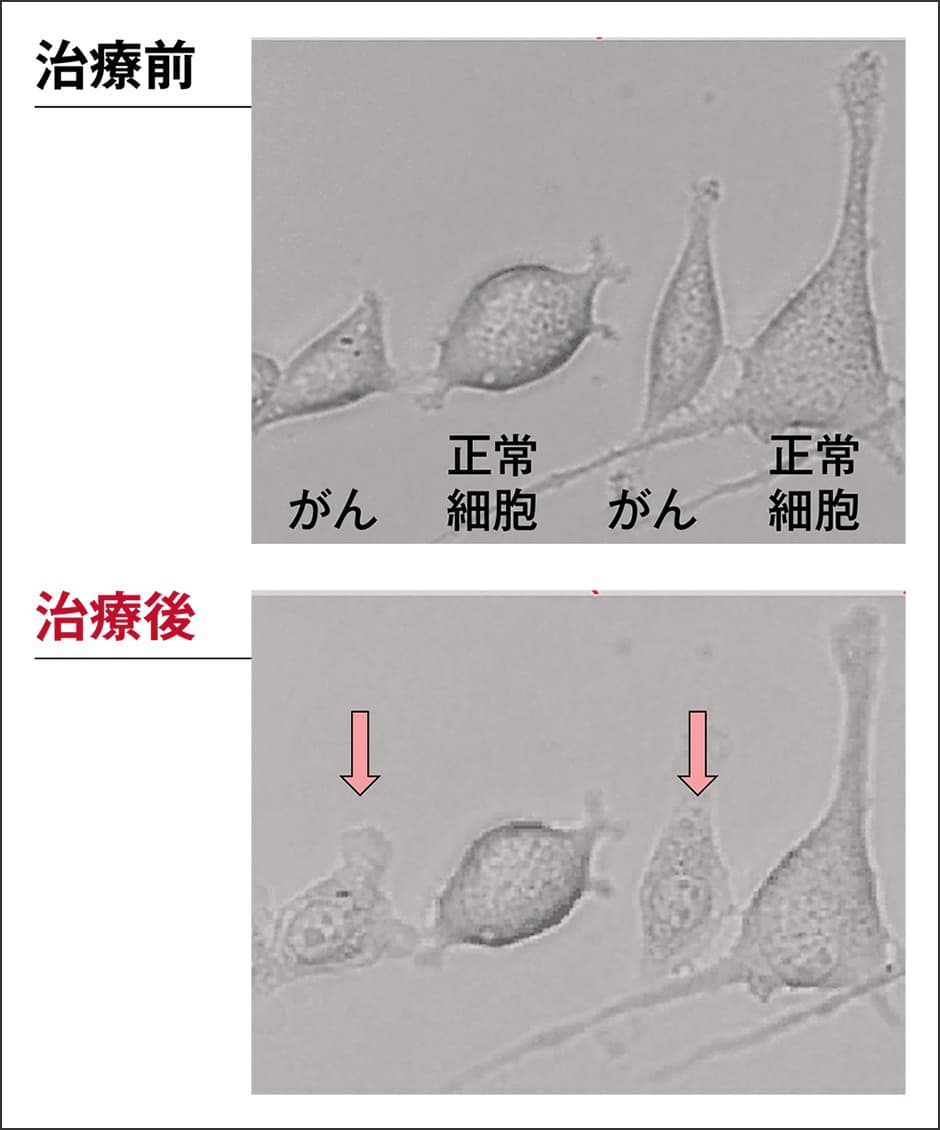
図2 治療前後の細胞の様子がん細胞は壊れて変形しているが、正常細胞には変化は見られない。
IR700は、体内に入ってがん細胞とくっつかなかった場合は、24時間以内に99%が尿から排出されてしまい、体に害を及ぼすということもありません。
こうして、がん細胞だけを選択的に殺し、正常細胞に障害を与えない、という光免疫療法の基本が確立したのです。
免疫の活性化にも非常に有効
光免疫療法が「免疫」を謳うのは、この療法ががん細胞を選択的に殺すだけでなく、免疫の活性化にも非常に有効だからです。
がん細胞は日常的に発生しており、その数は、研究者によって1日1000個とも5000個ともいわれています。それだけのがん細胞が発生しても“病気”とならないのは、私たちの体に備わる免疫機構によるものです。がん細胞は異物ですから、免疫細胞ががん細胞を認識して活性化すれば、退治されます。免疫ががん細胞を処理しきれなくなると、がんという病気になります。そこで、免疫細胞を増強するような治療法が開発されていますが、それらは制御が難しく、自己免疫疾患や臓器不全を起こすことがありました。むしろ、免疫の活性を促すためには、免疫細胞が、がんを「がん」だと認識できる状態にして、その役割を存分に果たせるようにすればよいのです。
光免疫療法では、いくつものがん細胞がみるみるうちに壊れると説明しましたが、このとき、壊れたがん細胞からは、内部のがんの特徴となる抗原を含む新鮮なタンパク質が大量に外部に放出されます。大量の抗原にさらされた近傍の樹状細胞(免疫細胞)は一気に活性化して抗原情報を獲得し、それをリンパ球(免疫細胞)に伝えます。リンパ球は活性化して分裂し、残っているがん細胞を攻撃し始めるのです。
「一気に大量に」抗原が出てきたときに反応するというのは、免疫の中でも最も基本的な機構であって、その点でも光免疫療法が免疫を活性化するのは非常に理にかなっているといえます。従来の治療法では、薬剤や放射線などによってがん細胞が変容するまで細胞膜が破れることはないので、細胞内のタンパク質もそのがんの特徴を維持したままでは放出されません。そのためがん細胞の特徴を認識することができなくなってしまうのです。
さらにこのような経過を経る免疫の活性化が、転移したがんにも有効に作用することも分かりました。
原発がんから転移したがんは、元のがんの特徴を持ちつつも、必ずしも同一ではありません。がん細胞は複数の遺伝子に変異が起きています。例えば、原発のがん細胞にA、B、C、Dという遺伝子の変異があっても、転移したがん細胞には、B、C、Dの変異しか見られないことがあります。もし、原発がんに使用した薬剤がAをターゲットにしていたとしたら、その変異を持たない転移がんは見逃されてしまうでしょう。
しかし、光免疫療法で活性化した免疫細胞は、A、B、C、Dすべての特徴を認識しています。すると、転移したがんがB、C、Dの特徴しか持たなかったとしても、これを攻撃対象として認識することができるのです。
現在、行われている光免疫療法では、切除不能な局所進行または局所再発の頭頸部がんに保険適用されています。適用範囲をさらに拡大するために、日本国内では十数カ所で治験を行っています。
治療成績は、最初の照射で80〜90%ほどのがんを破壊して死滅させ、それを数回繰り返すことで、通常ほぼすべてのがんを死滅させています。最初の照射でがんを100%死滅させる必要はありません。抗体がくっついて光を照射されたがんは即座に死滅しますし、それを受けて、免疫細胞はしっかりとがんの特徴を認識し、がん細胞への攻撃を始めることができるからです。また、従来の免疫療法においても、光免疫療法を併用して治療成績が上がるケースが多く出ています。
副作用としては、人によって、あるいは、がんの場所によって腫れや痛みといった炎症反応が起こることがあります。がん細胞が壊れ、死んだ細胞を処理する白血球が活性化するためです。その振る舞い自体、免疫が活性化することの証左であり、長く続くものではありませんが、痛みが強いときには鎮痛作用のある薬を使います。
また、皮膚を破っているような大きながんの場合、皮膚の幹細胞も残っていないことが多く、がん細胞が急に一気に死滅してしまうと創傷が治りにくいことがあります。
がん細胞を認識して攻撃を仕掛ける
免疫が適切に機能するために、制御性T細胞をがんの周囲でのみ排除する治験も進めています。
制御性T細胞は、自己や、自己以外でも本来攻撃対象とする必要のないターゲットに働く「自己免疫」を抑制しています。免疫の暴走を制御する、非常に重要な働きを担う細胞です。ところが、がん細胞は制御性T細胞のこの機能を巧みに利用し、がん細胞への免疫作用に非常に強い抑制をもたらしています。
そこで、制御性T細胞にのみ結合する抗体を投与し、がん周辺に近赤外光を照射します。すると、がん細胞が壊れるのと同様、制御性T細胞も壊れていきます。がん細胞は、制御性T細胞の守りがなくなり、周囲の攻撃性の免疫細胞は、がん細胞を認識して攻撃を仕掛けるようになるのです。しかも、光免疫療法は光エネルギーがなければ作動しない仕組みですから、がん以外に光を照射しなければ、他の場所にいる制御性T細胞にくっついている抗体には何も起こらず、自己免疫を起こすことにはならないのです。私は、この最終形の光免疫療法によってがんの8割までを完治させることを目標にしており、制御性T細胞をターゲットにした療法はそのための重要なピースとして治験を進めているところです(図3)。
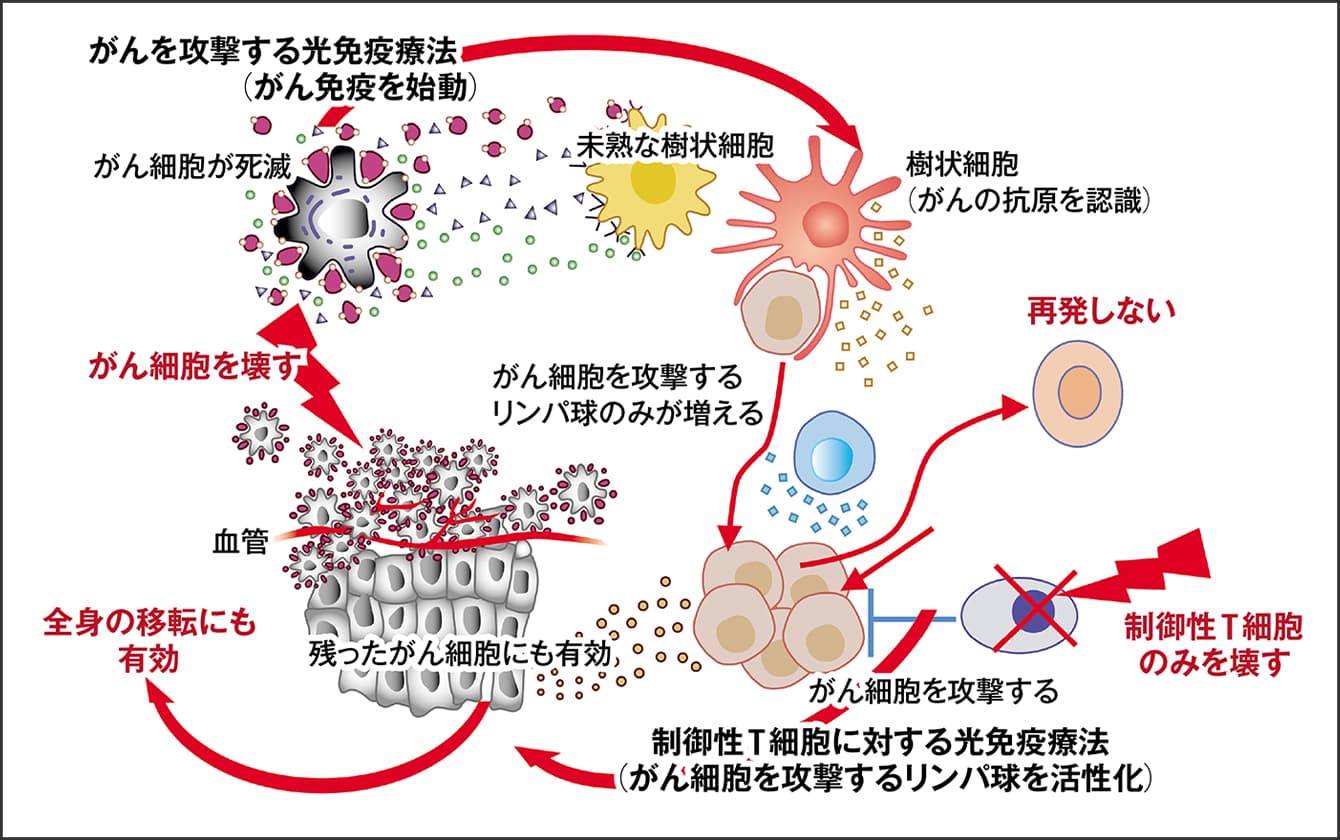
図3 光免疫療法の最終形がん細胞は、光エネルギーで作動する抗体複合体によって壊れる。その際、新鮮ながん細胞特異のタンパク質が大量に散らばり、周囲の免疫細胞ががん細胞を認識し活性化する。同様の仕組みを用い、免疫からがん細胞を守っていたがん細胞周辺の制御性T細胞を破壊し、がん細胞への攻撃を始める。がんの特徴をしっかりと認識した免疫細胞は、転移した細胞や治療耐性のある細胞をも認識して作用する。
正常細胞に障害を与えず、無害の薬と光を使ってがん細胞と免疫抑制細胞を選択的に殺し、免疫を活性化するという光免疫療法の論理はすでに確立されています。保険適用はまだ一部のがんにとどまっていますが、この治療法が広く普及するよう、尽力していきたいと思います。