がんによる体重減少は大きく分けて、がんが引き起こす炎症やホルモンの代謝異常が直接的な原因となる「誘発性」と、がんに罹患したことが間接的に影響する「関連性」の2パターンある。手術後に合併症が起きやすくなるなど、体重の減少が予後の悪化を招くという事例は数多く報告されている。体重減少が治療の継続性を左右することは明白で、今では低栄養を予防・改善することが、がん治療の重要なファクターとなっている。栄養治療はがん医療を支える重要な存在だ。
〈シリーズ〉がんから身をまもる
第5回 栄養治療 体重を減らさないこと! 筋肉量減少は治療に影響する
構成/飯塚りえ イラストレーション/小湊好治
がんの症状というと、多くの方は痩せること、体重減少を思い浮かべることでしょう。がんの体重減少は、がん誘発性とがん関連性との2種類に分けて考えられています。
がん誘発性の体重減少は、がん悪液質と呼ばれる、がん細胞によって引き起こされる炎症やホルモンの代謝異常による合併症が原因です。過去6カ月間の体重減少が5%を超えることが診断基準の一つとなります。悪液質まで進行すると、栄養補助剤などを用いても栄養状態を改善するのは簡単ではありません。
低栄養を予防することが大切
2つ目のがん関連性体重減少とは、がんになったことによって体重が減少する症状で、原因は、
1)がんが臓器を占拠するなどして食事の摂取、消化、吸収が困難になる
2)治療による影響や副作用によって食事の摂取が困難になる
3)告知でショックを受けるなどの心理的な問題
4)痛みや倦怠感などによる食物摂取量の低下
——が挙げられます。がん細胞そのものが悪さをしているのではなく、それぞれ、手術でがんを切除する、副作用を抑える薬を使う、カウンセリングを行う、などで改善することができます。がんの栄養治療はこれらを対象としており、がん誘発性の体重減少に至る前に、栄養状態を把握し、低栄養を予防することが大切です。
では、なぜ体重減少に留意しなくてはならないのでしょうか。それは体重減少によって、がんの治療成績が大いに左右されるからです。
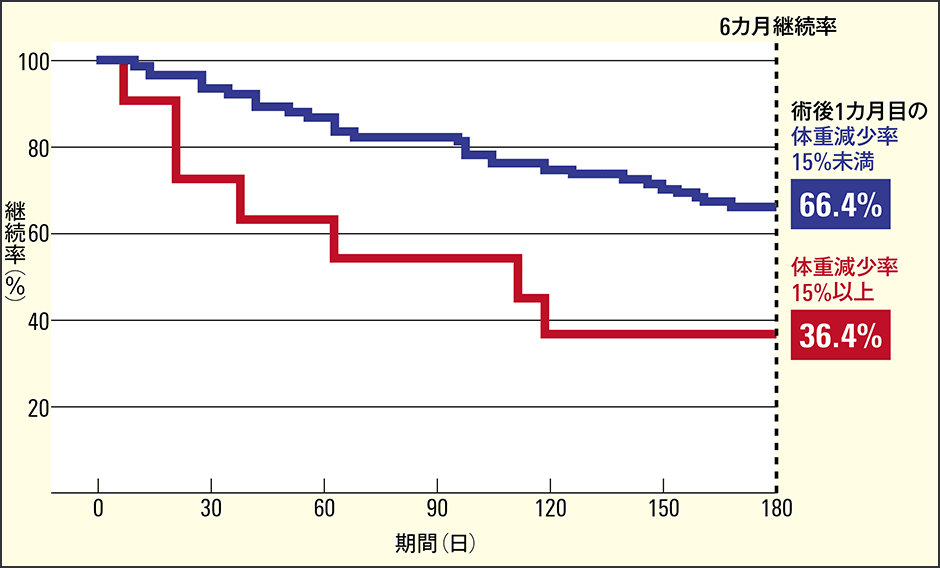
がんで手術をした後に、残ったがん細胞を殺傷するための補助化学療法を行うことがありますが、胃がん術後補助化学療法を行ううえで、手術による体重減少、特に筋肉量減少がその治療継続性に大きく影響するというデータがあります(図1)。
 Aoyama T, Yoshikawa T, et al. Body weight loss after surgery is an independent risk factor for continuation of S-1 adjuvant chemotherapy for gastric cancer. Ann Surg Oncol, 20: 2000-2006, 2013.
Aoyama T, Yoshikawa T, et al. Body weight loss after surgery is an independent risk factor for continuation of S-1 adjuvant chemotherapy for gastric cancer. Ann Surg Oncol, 20: 2000-2006, 2013.Aoyama T. Yoshikawa T, et al. Loss of Lean Body Mass as an Independent Risk Factor for Continuation of S-1 Adjuvant Chemotherapy for Gastric Cancer. Ann Surg Oncol, 22: 2560-2566, 2015.
図1 体重減少と抗がん剤継続率術後1カ月目の体重減少率が15%未満では、抗がん剤を6カ月継続して使用できた患者が66.4%だが、体重減少率が15%を超えると2カ月後の抗がん剤継続率が60%を切り、6カ月後には36.4%となる。
他にも、栄養状態が悪く体重が減少して手術後の合併症が起きやすくなったり、筋肉量が落ちた患者は予後が悪くなったりといったデータが次々に発表され、これまでになかったがんと栄養のエビデンスが積み重なってきました。体重を減らさないこと、そしてそのためのがん治療における栄養治療の役割の重要性が理解できると思います。
筋肉は栄養を蓄える重要な臓器
その中でも体重減少というとき、問題となるのは筋肉が減少してしまうことです。
人間の栄養、つまりエネルギー源の一つに、グリコーゲンがあります。グリコーゲンは、分解しやすく体が利用しやすいエネルギーですが、蓄えられる量が限られています。一方、エネルギー源としての脂肪は、分解に時間がかかり、即戦力とはなりがたいという性質があります。がんの治療ではグリコーゲンに焦点を当てています。
グリコーゲンの貯蔵庫は、主に肝臓と筋肉、特に腸腰筋、いわゆるコアマッスルです。それぞれに特徴があり、銀行に例えると、肝臓はキャッシュディスペンサー、筋肉は本店窓口のようなものです。そこから“栄養=グリコーゲン”を下ろして使っているとしましょう。
日常の買い物をするには、わざわざ本店の窓口で下ろすことは、ほぼありません。ディスペンサーで下ろします。しかし、ディスペンサーで下ろせる量には限りがあり、2日間程度で蓄えがなくなってしまうので、ディスペンサーたる肝臓は、本店窓口の筋肉から栄養を補給してもらいます。筋肉は栄養を蓄える重要な臓器だということです。
ところが、筋肉はさまざまな原因で失われます。30歳以降、1年で約1%の筋肉量が低下します。80歳になると、30歳のときと比較して約50%もの筋肉を失うことになります。入院で寝たきりの状態が続くなどして活動量が低下することでも筋肉量は低下します。一般に1週間の寝たきりで10〜15%の筋肉量が低下するといわれています。
さらに、がんの場合、慢性炎症の状態になりますし、手術による急性の炎症も避けられません。炎症には栄養を多く使い、いずれも筋肉量の低下を招きます。
がんに罹患するのは高齢者が多いのですが、すでに加齢による筋肉量の低下が起こっているところに、手術を受けたり入院で活動が低下したりすれば、筋肉量が急激に低下することが容易に想定できます。十分な栄養治療の必要性を特に感じます。
栄養状態が、想定を大きく超えて予後を左右することが分かってきた今、栄養治療とは、現状の低栄養を治療し、これから起こる可能性のある低栄養を予防することだと考えています。
世界では、主要な臨床栄養学会が、国際的な栄養対策における共通の基準の必要性を認識し、「GLIM基準(Global Leadership Initiative on Malnutrition)」として、成人の低栄養診断基準を提唱しました。日本でも「日本栄養治療学会(JSPEN)」が、この基準を推奨することとし、さらに厚生労働省も賛同して、2024年4月からこの基準を使った診断が保険適用となりました。入院患者にスクリーニングをして、低栄養の可能性のある患者にはこのGLIM基準を用いて、低栄養の診断を行います。
栄養という視点が現場には欠かせない
低栄養とさまざまな疾患とに深い関連性があることは、世界中から報告されるデータが示唆していますが、GLIM基準でスクリーニングを行って要注意となるのは、圧倒的に悪性腫瘍の患者です。がん患者と栄養という視点が、医療の現場に欠かせないことを実感しています。
がんの治療と栄養という視点から、興味深い例を挙げましょう。
がん研究会有明病院の布部創也先生が発表された論文によると、80歳以上の早期胃がん患者の場合、手術後に再発する患者はほぼいないにもかかわらず、胃の手術から数カ月後に、がん以外の理由で突然死される方が非常に多い、というのです。
原因は解明されておらず、今後の詳しい研究が必要ですが、私は糖尿病の患者に見られる心臓疾患が原因解明のヒントになるという仮説を立てています。
糖尿病の患者は、薬剤の影響で低血糖になることがあります。食事を摂った後の低血糖(食事性の低血糖)や、就寝中に低血糖が続く持続性低血糖(夜間低血糖)になることがあり、心筋梗塞との関連が指摘されています。食事性の低血糖は、あめなど甘い物をすぐに摂取すれば回復しますが、夜間低血糖は危険です。
夜間低血糖の状態では、血流を上げようとして交感神経が働き、基本的に副交感神経が支配している就寝中、突然に心臓が活発に動き出します。心臓の負担は大きく、高齢で心臓の血管が狭くなっているなどの場合、心筋梗塞を起こすといわれています。
これと同様の事象が、胃を摘出した患者にも起きているのではないかと考えました。
そこで、胃の手術をした患者に、糖尿病患者が使う、血糖をモニターする器具を装着してもらいました。するとやはり、これらの患者には糖尿病患者同様に、食事性の低血糖、夜間低血糖がともに見られたのです。つまり、胃がんの手術後に夜間低血糖に陥り、心筋梗塞を発症して亡くなったというストーリーが成り立つのです。
患者は、胃の手術をして食事を摂れず、先ほどのディスペンサーと本店窓口でいえば、どちらも蓄える機能はあるものの、十分な供給がないために栄養が不足し、夜間低血糖が起きていたと考えました。これには、肝硬変の低血糖への対応として行われているレイトイブニングスナックを参考に対処しました。レイトイブニングスナックは、寝る前に、チーズなど脂肪分の多い食物を摂ってもらう処置です。脂肪はグリコーゲンに比べて分解が遅いので、夜間低血糖が解消されるのです。胃の手術をした患者にも、これと同じように寝る前に、脂肪分を多く含む栄養剤などを補給してもらうと、夜間低血糖が一切なくなりました。
高齢者に多いとはいえ、若い患者にも起こります。実際、私の担当した40代の患者は、術前の検査では心臓を含めてまったく問題がなく手術も成功しましたが、数カ月後に突然死されました。胃の手術後の低血糖と心筋梗塞の関連を疑っていた矢先の出来事で、この例をきっかけに、何とかしなければと、レイトイブニングスナックのような治療を始めました。
胃の手術後の他病死を防ぐ手法として広く提唱するには症例数が不足しているのですが、今後、全国規模での研究を進めたいと考えています。
がんの治療における低栄養の予防には、さまざまなアプローチがありますが、消化器の専門医である私としては、外科手術、特に胃の切除に関して留意しなくてはならないと考えています。

切除後の状態を見ていかなければならない
胃がんになると、臓器を摘出する手術も少なくありません。
胃がんの種類の一つに、未分化がん、いわゆるスキルス胃がんがあります。胃の粘膜層に発生して細胞の形態が原始的なため、成熟したがんと比べて識別が難しく、かつ胃がんの中でも特に進行が早く予後も悪いがんです。そのため、このがんを疑うと早期であっても胃を全摘する手術が多く行われました。しかし、胃を全摘した患者は、がんは確かに完治したものの、食欲がなくなる、食事がおいしくない、などによって術後、体重が劇的に減少し、QOLがぐっと下がってしまうことを間近に見てきました。栄養障害によって筋肉も落ちてしまうので、がんは治っても、他の病気で亡くなるという可能性も高くなります。
全摘をすると、胃が袋としての機能を果たせなくなり、それが食欲不振の原因と考えがちですが、そうではないのです。それ以上に噴門を含む胃の上部が大切だったのです(図2)。
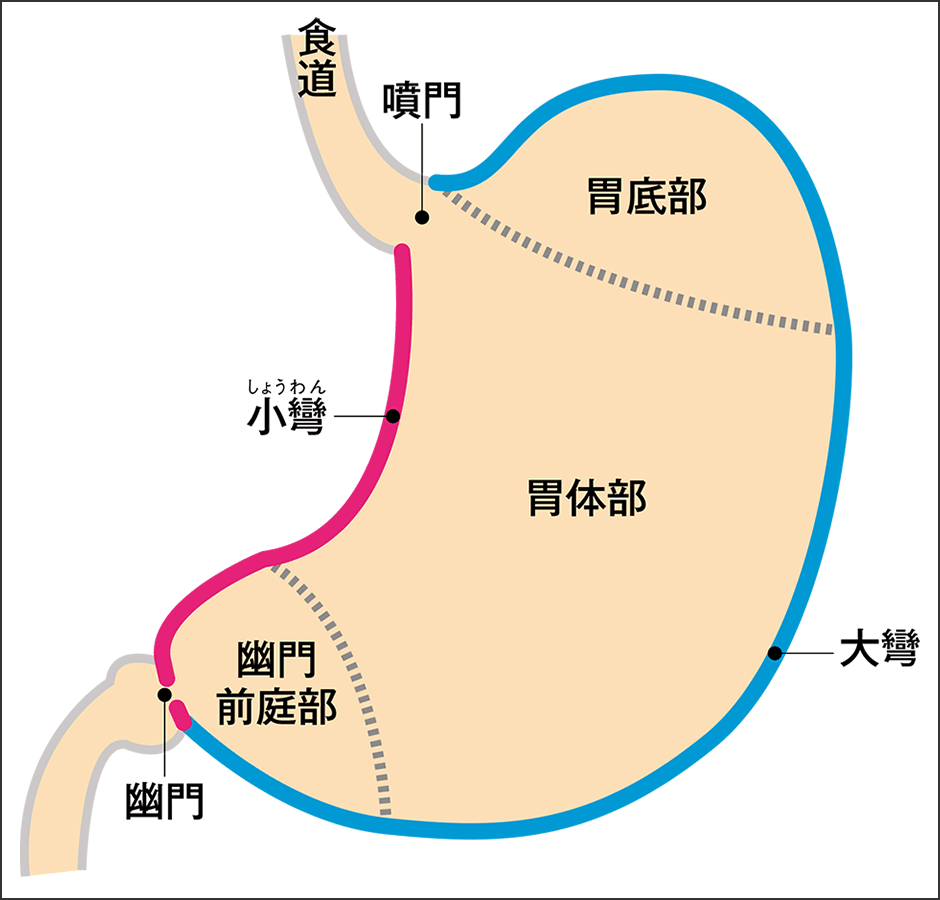
図2 胃各部位噴門は、食道とのつなぎ目にある胃の入り口。食物の通過を調節する役割とともに、食欲を促すグレリンを分泌する役割も大きい。
大きめの餃子くらいの部位ですが、ここからはグレリンというホルモンが分泌されます。また、グレリンは脳の視床下部に作用して成長ホルモンの分泌を促し食欲増進の働きがあるホルモンでもあります。成長ホルモンは、筋肉を増やす作用もあるので、体重の減少を防ぐことにも有効です。
そこで、この部位を残す術式を第1選択としてグレリンの分泌を維持しました。すると、術後、体重の減少は多少あっても筋肉は残るので、患者は活気もあり、元気に食事ができるようになりました。胃の全摘を行うと、従来は3カ月ほど経過してようやく術前の4割程度食べられるといったイメージですが、患者のこのような様子を見ると、胃は、食物の入れ物としての役割よりも、グレリンを分泌する役割のほうが大きいのかもしれないと感じています。
これらの例を踏まえ、私は、胃をホルモンの分泌臓器とも考え、胃の摘出後もグレリンの分泌を可能にする術式の開発、普及を目指しています。
これまでの治療は、がんを切除することに注力していた傾向がありますが、ここで述べてきたように、臓器を切除するとどうなるか、切除後、どのような状態になるかを見ていかないことには、結局、本当の治療にはなりません。
私は以前から、栄養を摂取することが治療において重要だという認識があったので、胃を全摘した後の栄養補給として経口栄養剤の摂取の有効性について、綿密なスタディを行ったことがあります。結果は、栄養剤にはまったく効果がなく、摂取してもしなくても体重は減少し筋肉量も減るというもので、がっかりしたという経験があります。栄養剤は補助的なものにはなるかもしれませんが、栄養の根本的解決には至らないということなのです。
というのも、患者は食欲がないので、前向きに摂取する気持ちにならず、意欲を失ってしまいます。考えてみれば、食は人生の大きな楽しみです。好きなものを好きなように食べるという意欲を残すことは生きるために欠かせず、それを奪うのは栄養治療において最悪の道筋です。栄養状況を無視したがん治療は危険だとすら考えるようになりました。がんは、外科手術、薬物療法、放射線療法が三大治療といわれていますが、それらの治療を根本から支えるのが栄養治療です。がんと栄養との関わりを真摯に捉え、栄養治療をがん治療のスキームに取り込む活動を続けています。
















