
がん化に関わる遺伝子が突然変異を起こし、それが蓄積することで正常細胞はがん細胞に変化する。近年の大規模がんゲノム解析で、さまざまな原因によって引き起こされる突然変異には「変異シグネチャー」と呼ばれる特有のパターンが50種類以上存在することが明らかになった。変異シグネチャーは喫煙や紫外線などの発がん要因と密接に関連していることから、解析が進めば危険因子を正確に特定することができ、発生メカニズムの解明にもつながると考えられている。
イラストレーション/北澤平祐

がん化に関わる遺伝子が突然変異を起こし、それが蓄積することで正常細胞はがん細胞に変化する。近年の大規模がんゲノム解析で、さまざまな原因によって引き起こされる突然変異には「変異シグネチャー」と呼ばれる特有のパターンが50種類以上存在することが明らかになった。変異シグネチャーは喫煙や紫外線などの発がん要因と密接に関連していることから、解析が進めば危険因子を正確に特定することができ、発生メカニズムの解明にもつながると考えられている。
日本人は世界でも平均寿命が長い長寿の国であるが、同時にがん大国でもある。日本人の2人に1人ががんにかかる、というデータはよく耳にするだろう。そのがんについて、世界では類を見ない日本人特有の特徴があることが最近明らかになってきている。
「我々も想像もしていなかったのですが、最新の研究から日本人に特徴的ながんの原因があることが見えてきました」
東京大学医科学研究所ゲノム医科学分野教授の柴田龍弘氏はそう話す。柴田氏らが参加する国際研究チームは2024年に、日本を含む11カ国の国際共同研究による過去最大の962例の腎細胞がんの全ゲノム解析を行い、日本人の腎細胞がん患者の約7割に、他国ではほとんど見られない遺伝子変異パターンが見つかったという論文を発表した。
「腎臓がんの原因は、実はまだはっきりと解明されていません。疫学研究によると、高血圧や糖尿病、肥満などが腎臓がんのリスク要因であることは分かっています。しかし、これらだけが原因なのかどうかは明確ではない。そこで原因を詳しく調べるために、世界中から集めた腎臓がんのサンプルを使い、ゲノム解析を行ったわけです」
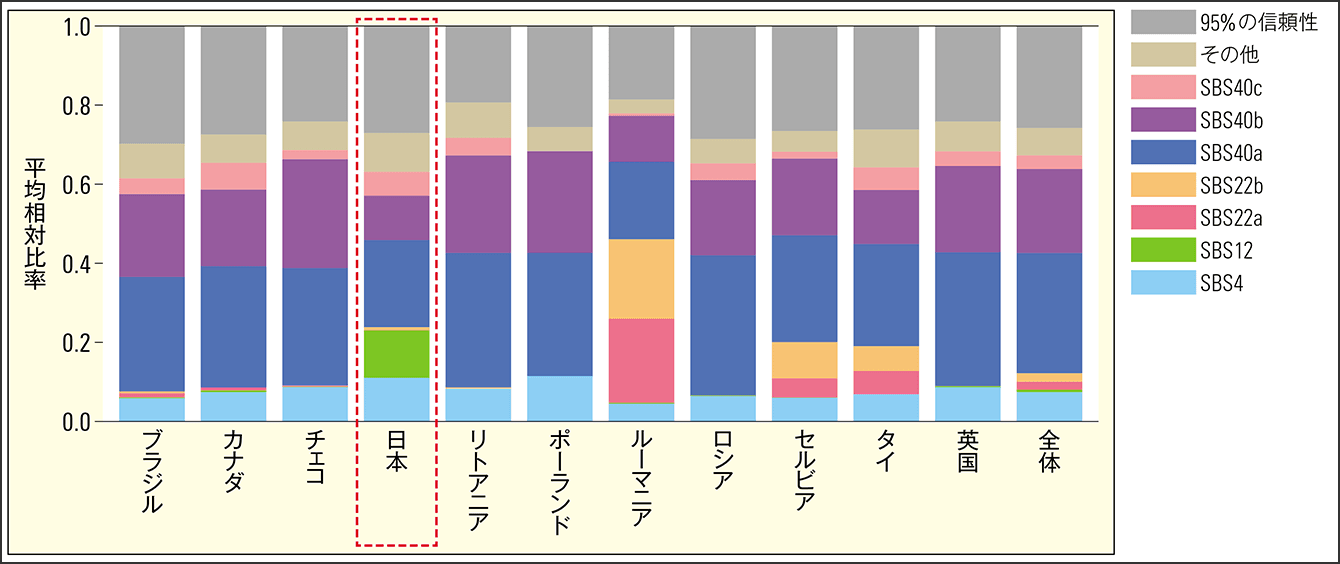
ゲノム解析の結果、誰も予想していなかった事実が明らかになる。日本人の症例のみに見られる「ユニークなパターン」が見つかったのだ。そのパターンは日本人の症例の約70%に見られた一方、他国の症例では2%程度という非常にまれなものだった(図1)。
 東京大学医科学研究所 2024年5月14日プレスリリースを改変
東京大学医科学研究所 2024年5月14日プレスリリースを改変
図1 腎細胞がんにおける国別の変異シグネチャー(SBS)の分布日本人の症例の約7割にSBS12が検出されたが、他の国では2%程度しか見られない。
そもそも、がんは遺伝子(ゲノム)の病気であることが分かっている。がん細胞の増殖や転移を促進する「がん遺伝子」と、それを抑制する「がん抑制遺伝子」があり、これらは「がんドライバー遺伝子」と呼ばれる。このドライバー遺伝子が突然変異によって異常を起こすことでがんが発生したり進展したりする。
「がんのゲノム解析では、どの遺伝子に異常があるのかを明らかにすることがとても重要です。同時に我々は、そのゲノム情報を基に、このがんがどのようにして発生したのかという原因を解明する研究も行っています」
国際的な研究による大規模ながんゲノム解析の結果、がん細胞のゲノム異常である突然変異には、その原因ごとに特有のパターンがあることが分かってきた。このパターンは「変異シグネチャー」と呼ばれる。
「これまでの研究により、喫煙や紫外線、遺伝的要因などに関連する50種類以上の変異シグネチャーが確認されています。しかし、そのうちの約3分の1はいまだに原因が明らかになっていません。つまり、我々がまだ知らない、がんのリスクを高める要因がまだまだ存在しているんですね。がんゲノムの研究を通じて、これらの未知の要因を解明することで、将来的にはがんの予防に大きく貢献できると期待しています」
では、この変異シグネチャーとは具体的にどのようなものなのか。例えば、喫煙が原因でがんが発生する場合と、紫外線が原因の場合では、ゲノムに起こる異常の場所が異なる。
今回の研究で見つかった腎細胞がんにおける変異シグネチャーはSBS12と呼ばれるもので、この日本人特有のパターンは原因が未知のものであったと柴田氏は話す。
「実は私たちは過去の研究において、このSBS12というパターンが肝臓がんでも多く見られることを発見していました。しかし、その際に日本と欧米との比較は行っておらず、まさか欧米ではほとんど見られないとは思っていなかったのです。最新の研究ではこのパターンが日本人に特に多く見られ、非常に特異的であることが明らかになりました」
つまり、肝臓がんも日本人に特異的な要因があるということが、ゲノムのデータ解析により見えてきたというわけである。この成果を踏まえ、今後はアジアの他の国や、日本の中でも地域差があるのかを調べ、その未知の原因を突き止める研究を進めていくという。
「今回の国際共同研究では日本国内における分布については十分解明できていません。そこで現在、国内から広く症例を集めて研究を進めています。その理由は2つあります。1つ目は、今回見つかった変異シグネチャーの分布状況を正確に把握するためです。2つ目は、こうした分布の違いを分析することで、その原因の解明につながる可能性があるからです」
現時点で明らかになっているのは、原因は未知とはいえ、それが外因性の発がん物質、環境要因である可能性が高いということだ。
外因性というと、喫煙や紫外線、放射線などが知られているが、他にはどんなものがあるのだろうか。
「日本人に特有のがんの原因については、食生活や生活習慣、環境要因などさまざまな可能性を指摘する人もいます。しかし、実際のところ、その原因はまだまったく分かっていません。今後、さまざまな方法を使って詳しく調べていく予定です」
多くの発がん物質は、原因となる化学物質が細胞内に取り込まれ、DNAに結合する。この結合がDNAの複製過程でエラーを引き起こすため、突然変異が生じる。よって、DNAに結合している物質を特定できれば、それがどのような化学物質に由来するのかを推測することが可能になるという(図2)。
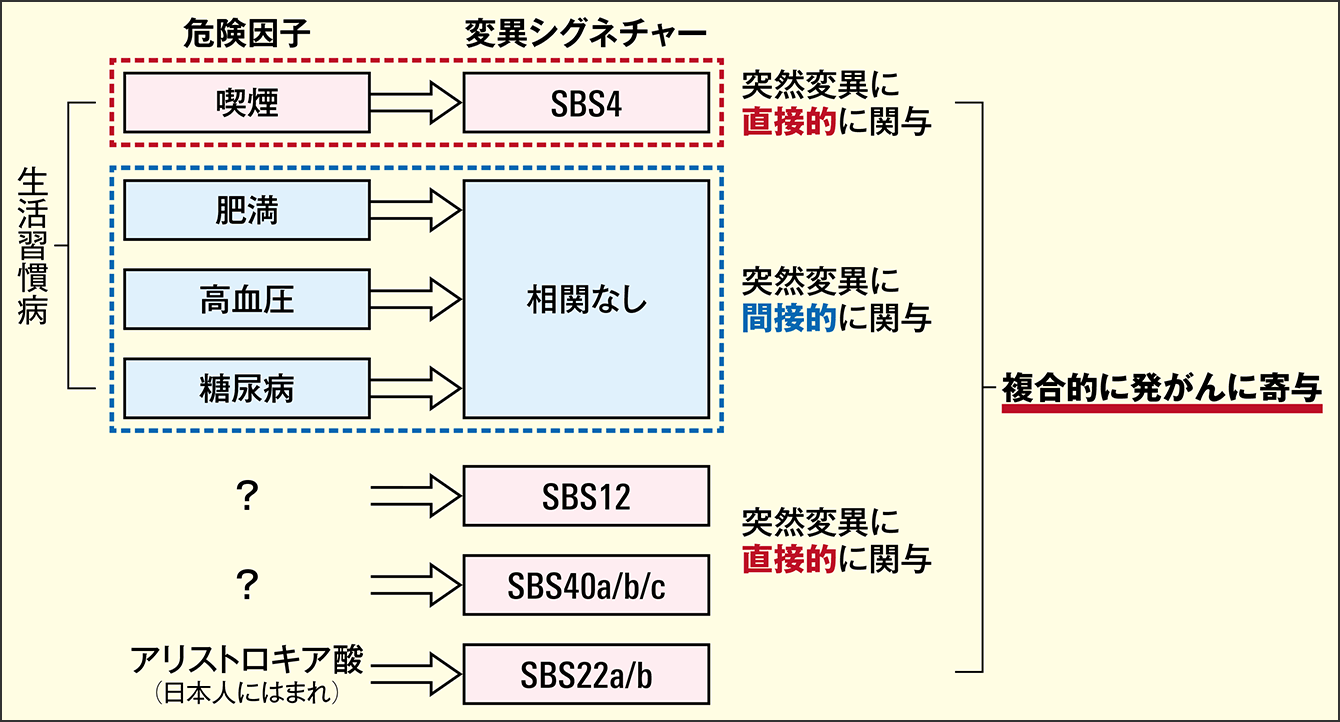
図2 腎細胞がんの危険因子が発がんに至るメカニズムゲノム解析によって発見された変異シグネチャーは、危険因子によってそれぞれ発がんに至るメカニズムが異なることが明らかになった。
ちなみに、海外では次のような発がん物質が見つかった例もある。腎臓がんや肝臓がんの危険因子として知られるアリストロキア酸が、一部の漢方薬に含まれていたというのだ。
「台湾では肝臓がんの約8割の症例がこのアリストロキア酸による変異パターンを示していました。おそらく漢方薬などを通じてアリストロキア酸を摂取した人が結果としてがんを発症したと考えられます。現在、台湾ではアリストロキア酸が含まれる漢方薬の製造は禁止されています。この事例から言えるのは、原因を正確に特定できれば、がんの予防につなげられるということです」
日本ではそもそもアリストロキア酸が含まれた漢方薬は製造も輸入も禁止されている。ただし、少ないながらも個人輸入などで手に入れる人もいる。
「繰り返しになりますが、我々も日本人特有の腎臓がんの原因があるとは、予想もしていませんでした。泌尿器科などの専門家に尋ねても皆さん口をそろえて『予想もしなかったし、原因は考えつかない』とおっしゃいます。現時点では、候補らしいものは一切思い浮かばない状態です」
日本人に多い変異パターンは他にもある。それはアルコール飲酒に関係する変異のパターンである。柴田氏を中心とする研究チームは、2023年に日本人の胃がんのゲノム解析を行い、予後不良として知られるびまん型胃がんについて飲酒との関連を初めて発見した。
胃がんは日本人の罹患数が3位で、死亡数は4位である。これまで胃がんといえば、ピロリ菌が発がん要因としてよく知られていた。その一方で、悪性度の高いびまん型胃がんについては未解明だったという。
「海外の人々もお酒を飲んでいるにもかかわらず、なぜ日本人だけが特定のパターンを示すのか。その理由の一つとして、日本人にはお酒に弱い人が多いことが挙げられます。研究によると、同じ量のお酒を飲んでいても、お酒に弱い日本人はアルコールに関連する異常が起こりやすいことが分かっています。これが、日本人特有のパターンが現れる一因と考えられています」
ここで発見されたSBS16という変異シグネチャーは、東アジアの人種に多く、男性、飲酒量、アルコールを代謝しにくい体質と有意な相関関係を示したという。
「アルコールに関する体質は大きく分けて3種類あります。まったく飲めない人、少し飲める人、そして飲める人です。特に問題なのは、少し飲める人です。この『少し飲める人』が慢性的にお酒を飲むと、胃がんや肝臓がんのリスクが高まることが研究から明らかになりました」
このアルコール代謝に関連するALDH2遺伝子多型は、アジアに特に多いことが分かっているという。
アジアでこの遺伝子多型が生き残り、増加している背景には何らかのメリットがあると柴田氏は指摘する。
「一説では、田植えの際にかかるツツガムシ病に対する耐性が関連しているのではないかとされていますが、よく分かっていません。この遺伝子多型が、がんリスクと関連しつつもアジアで正の選択を受けたとすれば興味深いですね」
柴田氏はがんの原因解明の重要性について、次のように話した。
「喫煙が原因でがんになる場合もありますが、それだけではなく、加齢による不可避なエラーも関与しています。原因を突き止めたとしても、必ずしも簡単に予防に結びつくとは限りません。しかし、その原因を明らかにすることで将来の患者を少しでも減らすことに貢献したいと考えています。これまでお話ししたように、日本人のがんの特徴を解明することが私の研究の大きな柱です。それが薬や予防法の開発につながり、最終的に患者さんの役に立つ方向へ広がっていけばと思っています」
実際に柴田氏らのゲノム解析の研究により、胆道がんの新しい治療標的となるドライバー遺伝子が発見され、治療薬が承認された。このようにゲノム解析の技術は、医療への実装に向けて進化を続けている。ただし、まだがんの遺伝子に関しては解明されていない部分が多いと柴田氏は言う。
「がんのタンパク質をコードする遺伝子についてはかなりの部分が解明されています。しかし、ゲノム全体の95%以上を占める非コード領域と呼ばれる部分については、まだ十分に分かっていません。こうした基礎研究を続けることが、将来の大きな進展につながると考えています」
柴田氏の研究は、がんの発生メカニズムを遺伝子レベルで解明し、その知見を実際の医療に役立てようというものだ。そのようにがん研究の未来を切り開こうとする原動力とは、どのようなものなのだろうか。
柴田氏は東京大学医学部を卒業後、病理診断の道に進み、国立がん研究センター、東京大学で研究を続けてきた。まさにがんゲノム一筋の最先端の研究を行ってきた柴田氏は、「がんとはやはり生命の一つの表れだと思うんです」と語った。
「がん細胞にとって、がん治療は非常に大きなストレスとなります。そのような環境の中で、生き延びる方法を模索しているがん細胞の姿は、生物が進化の過程でさまざまな環境の変化に適応してきた過程と似ているといえます。がん細胞もまた、自分のゲノムを変化させることで進化するという生命現象の一つとして捉えることができます」
そのがんのゲノムを研究することで、新たな生命の原理が明らかになるかもしれない―。そう語る柴田氏にとって、がんは生命を理解するうえで非常に貴重な研究材料でもあるのだ。
「もちろん、がんを治療し克服することが最優先であることに変わりはありません。しかし同時に、がんの研究は生命そのものを深く理解するための重要な鍵にもなるのです」