
CAR-T(カーティー)細胞療法は、T細胞の遺伝子を改変することでがん細胞への攻撃力を増強する治療法で、がんとの共生を可能にする画期的な手法として注目されている。血液がんでは高い治療効果を発揮しているものの、塊をつくって防御する固形がんを攻撃することは難しく、苦戦を強いられてきた。しかしそのハードルもやがてクリアできるはずだ。CAR-T細胞は長期間がんを攻撃する能力を持つ。がんと共生する時代がいよいよやってくるかもしれない。
イラストレーション/北澤平祐

CAR-T(カーティー)細胞療法は、T細胞の遺伝子を改変することでがん細胞への攻撃力を増強する治療法で、がんとの共生を可能にする画期的な手法として注目されている。血液がんでは高い治療効果を発揮しているものの、塊をつくって防御する固形がんを攻撃することは難しく、苦戦を強いられてきた。しかしそのハードルもやがてクリアできるはずだ。CAR-T細胞は長期間がんを攻撃する能力を持つ。がんと共生する時代がいよいよやってくるかもしれない。
日本では2人に1人はがんと診断され、3人から4人に1人はがんで亡くなる。がん撲滅は人類の悲願とされてきたが、必ずしも制圧しなくてもがんと共生できる未来もあるかもしれない。
現在、がん治療の最前線として各国が開発にしのぎを削っているのがCAR-T細胞療法である。免疫細胞であるT細胞の遺伝子を改変して、がんへの攻撃力を増強する新しい治療法で、日本でも複数のCAR-T細胞が血液のがんで薬事承認されている。
山口大学大学院医学系研究科の玉田耕治教授はこう語る。
「これまでの治療法、例えば白血病であれば抗がん剤を使ったり、骨髄移植をしたりしても、どうしても効かなかったり再発したりする人たちに対して、CAR-T細胞を投与すると、約6割から7割の患者さんでがんが体の中から消えるというデータがあります。これは非常に治療効果が高いものです」
どのような仕組みによって実現されたのだろうか。
「人間の体の中にはいろいろな免疫細胞があって、それらががんを攻撃する力を持っています。がんができても免疫がきちんと働いてくれればよいのですが、攻撃できずにコントロールできない状況になってしまうと、がんという病気になります。つまり、免疫細胞はもともとがんを攻撃する能力を持っているけれど十分ではない。キメラ抗原受容体=CARというのは、がんを攻撃する免疫細胞の力が十分ではないところを強くして、きちんとがんを殺すように変えてあげるためのシステムです」
遺伝子組み換え技術を使って、T細胞にCARという遺伝子を組み込むことで免疫細胞の力は増強するという(図1)。この遺伝子は人間が持っているものではなく、人工的に作り出したものである。このCARには大きく2つの働きがあるという。
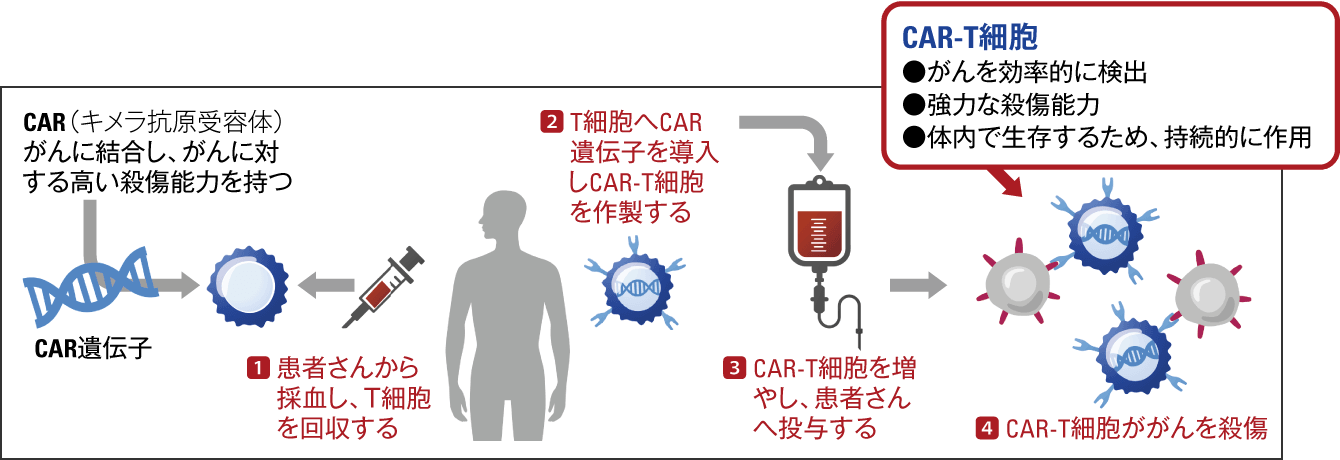
図1 最新のがん免疫療法:CAR-T細胞療法CAR-T細胞療法は、がんを効率的に検出し、強力ながん殺傷効果を持つ細胞を人工的に作製して投与する治療法である。
「1つ目は、がんを見つけてくれるアンテナのようなものを免疫細胞の外側に出す働きです。それによって、今まではがんを見つける力がなかったT細胞が非常に効率的に見つけることができるようになります。もう一つ、CARは細胞の内側と外側にまたがるような構造をしているのですが、外側のアンテナに加え、内側にはがんを見つけると、T細胞を活性化してどんどん増殖させ、がんを殺す能力を高めるようなシグナルが入る特殊な配列を持っています。こういう構造をしているので、通常の免疫細胞ではがんを見つけることができない、見つけても免疫細胞を活性化することができないという状況だったものでも、非常に効率的にがんを見つけ、免疫細胞を活性化して、がんを殺す力をつけることができます。今までだったら免疫細胞は、がんと竹やりで一生懸命戦っているような状況だったのが、そこに非常に強力な武器を細胞に与えて、例えばライフルとかショットガンみたいな感じで攻撃できるようにするものです」
最初にCARというアイデアが登場したのは30年ほど前の1990年代のことである。ただし、当時のCARの構造は十分につくり込まれたものではなかったため、あまり効果が出ておらず、今のような効果の見られる構造ができたのは2000年以降だという。
これまでに治療効果が確認されたのは血液がんであり、固形がんへの効果ははっきりしていなかった。しかし、がんのうち血液がんは数%程度で、残りの90%以上は固形がん、例えば乳がんや胃がんなど、血液ではない細胞に由来するがんである。どうやれば固形がんでもCAR-T細胞が効果を発揮できるのかを玉田教授は10年以上研究してきた。研究は、なぜCAR-T細胞は血液がんで効果があるのに、固形がんでは効果が出ないのかというところから始まった。
「血液がんはもともと血液の細胞ががん化しているもので、がんは血管の中を流れていたり、リンパ節や骨髄の中にあるため、それぞれが孤立して存在しています。CAR-T細胞もそうで、言ってみればがんとCAR-T細胞は一騎打ちしているような状態です。1対1ならCAR-T細胞は非常に強力な武器を持っているので、がんを殺すことができる。ところが固形がんは血管の中にはなく、臓器のところで塊をつくって増えているので、相手は城の中に立てこもっているような感じで、1対1の戦いにならない。そこにいくらショットガンを撃ち込んでもかなわないのです」
玉田教授の研究グループは、塊をつくっている固形がんに、どうやったらCAR-T細胞がより多く集まり、かつがんを攻撃できるのかを検討したという。まずは、免疫細胞ががんの塊の中に入っていけなければ、いくら外から攻撃しても勝ち目がないと考えた。
「投与したCAR-T細胞が固形がんに入っていくにはまずどういうシステムが必要かを第一に考えました。第二に、入っていったとしても、CARががんを見つけてくれないと意味がないのですが、比較的均一な特徴を持つ細胞である血液がんと違って、固形がんは不均一な細胞の集まりで、CARのアンテナでは検出できないようながんも存在するので見つけにくい。その2点が解決すべき課題だと明らかになってきました」
教科書に書いてあるような基本まで立ち返って洞察したことが大きなブレークスルーにつながった。
「私は教授として大学の授業で免疫学を教えていますが、その中でリンパ節の構造なども教えています。リンパ節の中にはCAR-T細胞のもととなるT細胞やそれ以外の免疫細胞であるB細胞などが存在していますが、リンパ節を顕微鏡で見てみるとT細胞はある特定の領域に集まっていることがわかります。そのような部分をT細胞領域と呼びますが、そこにT細胞が集まるためには何らかのメカニズムがあるはずで、そのメカニズムをCAR-T細胞に応用すれば、CAR-T細胞ががんのところに集まる方法もつくれるのではないかと考えました」
T細胞領域にT細胞が集まる理由には、CCL19というケモカインとIL-7というサイトカインの2つのファクターが重要であることは、これまでの論文から示唆されていたという。しかし、これまでは誰もそれをCAR-T細胞に応用しようとは考えなかった。
「このメカニズムをCAR-T細胞に応用すれば、リンパ節でT細胞が集まっているような状況が固形がんの中でもできるのではないかと思い至りました。数多くあるサイトカインやケモカインからなぜCCL19とIL-7を選んだのですかとよく聞かれますが、私がこの組み合わせを選んだというよりは、進化の過程においてリンパ節にT細胞が集まるために必要とされ、自然に選ばれた組み合わせがCCL19とIL-7であったということであり、それをCAR-T細胞に応用したわけです」
CCL19はがんの中に免疫細胞が入っていくときに重要な働きをするケモカインである。一方、IL-7は免疫細胞を活性化し、長期の記憶を獲得してがんを攻撃し続けてくれるようにするサイトカインである。
「CAR-T細胞がCCL19とIL-7の両方をつくることにより、塊をつくっているがんに、CAR-T細胞だけでなく他の免疫細胞も集まり、活性化させることができます。そしてCAR-T細胞だけでは見つけることができないがんでも、他の免疫細胞が見つけて攻撃してくれます。我々はこのようなシステムを作り出し、PRIME技術、PRIME CAR-T細胞という名称を付けました」(図2)
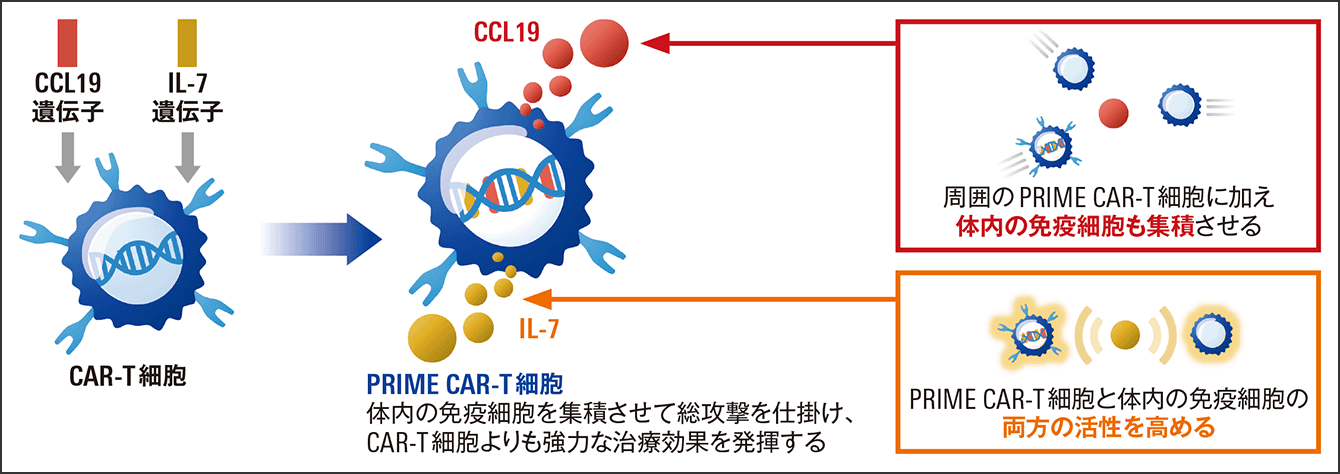
図2 PRIME CAR-T細胞とは免疫調整物質を産生するよう遺伝子を操作し、CAR-T細胞と体内の免疫細胞の集積と活性を高めている。
実際に、CAR-T細胞にCCL19とIL-7の遺伝子を追加で組み込んで、固形がんを持っている動物に投与してみると、がんの中に多くのT細胞が集まっていることがわかった。さらに、投与したCAR-T細胞だけでなく、体の中にもともとあるT細胞もがんの中に集まってきていることが見つかったという。
「マウスを使った動物モデルでは、7~8㎜の大きさの固形がんに対して、普通のCAR-T細胞ではほとんど効かずにがんが大きくなってマウスが死亡するような状況において、我々のPRIME CAR-T細胞を投与するとほぼすべてのマウスでがんが消失しました」
現在は、PRIME CAR-T細胞による治療を実用化するために、がん患者に投与する第Ⅰ相臨床試験を行っているという。玉田教授はさらに先を見据えている。
「今承認されているCAR-T細胞はすべて患者さん自身のT細胞からつくられていて、自家CAR-T細胞といいます。自家CAR-T細胞では患者さん自身の血液を取り出してCAR遺伝子の導入を行い、それを患者さんにまた投与しています。患者さん自身の血液なので使いやすいのですが、投与するまでに数週間もかかってしまい、その間にがんが進行してしまう心配があります。また、費用も1人3000万円以上と高額になります。一方で、他人の血液から取ってきたT細胞からCAR-T細胞をつくるものを他家CAR-T細胞といい、事前につくっておいてストックしておくことができますので、患者さんにすぐに投与できますし、費用も削減できます。ただし、他家の場合に難しいのは、他人の免疫細胞を投与することで起きてしまう拒絶反応で、できるだけそれが起きないようにする技術について世界中の科学者が研究しています。我々もゲノム編集技術という方法を使い、もっと強力で汎用性の高い他家のPRIME CAR-T細胞をつくろうと研究しています」
それにしても世界中の研究者が競っている固形がんに対するCAR-T細胞療法だが、玉田教授が独創的な研究をできた理由は何だろうか。
「独創的というと、何もないところから突然出てきたイメージですけど、ちゃんとした知識に基づいているものです。CCL19とIL-7の組み合わせは独創的なものを思いついたわけではなくて、こういうものが重要だということが人体の中ですでに示唆されていて、その知識を発想の転換で別のところにつなげたわけです。がんを治すということが目的であったとしても、その外側、アウト・オブ・ザ・ボックスといいますか、そこにも重要なヒントがたくさん存在していて、それらをどうやって自分の目標に転換していくかという発想が独創性の源だと思います」
もちろん、優れた発想があったとしても、それを実現するためには最先端の技術が必要だ。
「車の渋滞がひどいときに車が空を飛べたらいいなというアイデアは思いついても、現時点の技術ではすぐにそれはかないません。同じように、CCL19とIL-7でT細胞を集めるというアイデアを思いついても、それを組み込む技術がないと実現できません。そこにCAR-T細胞という技術があり、遺伝子組み換えという技術があったからこそ、かなえることができたのです」
CAR-T細胞療法は単なるがん治療ではない。玉田教授はがんとの付き合い方を変える未来像を描いている。
「今のがん治療は、いったん治療を始めたらなかなか社会復帰できないところがあります。会社を休職して、非常につらい抗がん剤の副作用と闘いながら治療を続けなければならず、経済的なダメージも非常に大きい。PRIME CAR-T細胞のように免疫の力でがんを長期間コントロールできるようになれば、がんと共存しながら社会生活を続けられるようになるのではないか、と期待しています」
CAR-T細胞は1回投与すると、体内にずっと残ってがんを攻撃すると考えられている。今年2月にNature誌に掲載されたアメリカの研究グループによる論文では、2010年ごろに治療を受けた白血病の患者の体内に、10年以上たった今でもCAR-T細胞が検出できたという。
「抗がん剤には半減期があり、それを過ぎると効果が弱くなるために何度も繰り返し投与する必要があります。抗体の治療でも同じです。ところがCAR-Tは細胞ですから、それ自体が生きている。うまくいけば投与した細胞がずっと生き延びて、10年以上ずっとがんの再発を予防してくれることもあり得るのです」
例えば子どものときに麻疹や風疹などの予防接種を打つと、その人は長い間その病気にかからない。ワクチンに対して免疫細胞が反応して、その免疫細胞がずっと体の中に記憶として残っているからだ。CAR-T細胞もそのようなメモリー細胞になっている。
「CAR-T細胞が、がんが増殖したり転移したりするのを予防してくれる。そうであれば、がんが完全に消えなかったとしても、うまく共存、共生できるようになるかもしれない。ちゃんと社会復帰して、元通りの日常生活を送ることができれば、がんがあっても不幸ではないかもしれない。例えば、高血圧と診断されても薬でちゃんと血圧がコントロールできて、最終的には寿命を全うできる方もいることと同じように、がんも怖くない病気になればと思います。がんと診断されても健康寿命を全うできる社会をつくり、患者さんが幸せな日常生活を取り戻せるようにしたい。それが我々の重要なゴールだと思っています」