
がん遺伝子の活性化や過度なストレスなどによってDNAが大きな損傷を受けたとき、細胞は自らを破壊してがん化を防ぐ(アポトーシス)。また、細胞分裂を停止したものの死なずに体内に長期間存在し続ける細胞老化も同様に機能する。しかしこの細胞老化の最大の問題点は、さまざまな炎症性物質を分泌するSASPを誘引することで、加齢性疾患を招き、高齢者や糖尿病などの人でCOVID-19が重症化しやすくなったり、後遺症の要因になったりするという。
イラストレーション/北澤平祐

がん遺伝子の活性化や過度なストレスなどによってDNAが大きな損傷を受けたとき、細胞は自らを破壊してがん化を防ぐ(アポトーシス)。また、細胞分裂を停止したものの死なずに体内に長期間存在し続ける細胞老化も同様に機能する。しかしこの細胞老化の最大の問題点は、さまざまな炎症性物質を分泌するSASPを誘引することで、加齢性疾患を招き、高齢者や糖尿病などの人でCOVID-19が重症化しやすくなったり、後遺症の要因になったりするという。
新型コロナウイルスの感染者数は全世界で6億人に達しようとしている。国内外の調査によると、そのうちかなりの人が、ウイルスが検出されなくなった後も後遺症、例えば倦怠感、呼吸困難、関節痛、味覚障害、脱毛など多岐にわたる症状に悩まされているという。
しかし、2年以上前から問題視され、これほど多くの人に影響を与えているにもかかわらず、後遺症のメカニズムはよくわかっていなかった。その謎をひもとく一つとして「細胞老化」があるのではないか。この研究を行った大阪大学微生物学研究所の原英二教授は次のように話す。
「新型コロナウイルスに感染すると、感染した細胞はしばらくたったらほとんどが死にますが、細胞が死ぬ直前に放出した炎症性サイトカインによって、周囲の非感染細胞が細胞老化を起こすことが我々の研究からわかりました」
これまで細胞老化は、がん遺伝子の活性化や過度な酸化ストレス、テロメアが短くなるなどによって引き起こされる過度なDNA損傷が原因だとされてきた。それに加えて、ウイルスによっても細胞老化が引き起こされることが明らかになった。
細胞老化とは、細胞が不可逆的に細胞分裂を停止してしまう状態を指し、そのような細胞を老化細胞という。
細胞には能動的な死としてのアポトーシスがある。異常を持った細胞が増殖してがん化することを防ぐためのプログラムという点では、アポトーシスと細胞老化は同じだ。一方で、細胞老化はアポトーシスとは違い、細胞がすぐに死ぬことなく、体内に老化細胞が長期間存在し続ける。
細胞老化の最大の問題点は、単に増殖を停止するだけではなく、炎症性サイトカインやケモカインなどさまざまな炎症性物質を分泌する細胞老化随伴分泌現象(Senescence-associated secretory phenotype:SASP)という現象を引き起こすことだという。老化細胞が蓄積して過度のSASPを引き起こすことにより、慢性炎症が起きたり、がん、心血管疾患、糖尿病、アルツハイマー型認知症など加齢性疾患になりやすくなると原教授は言う。
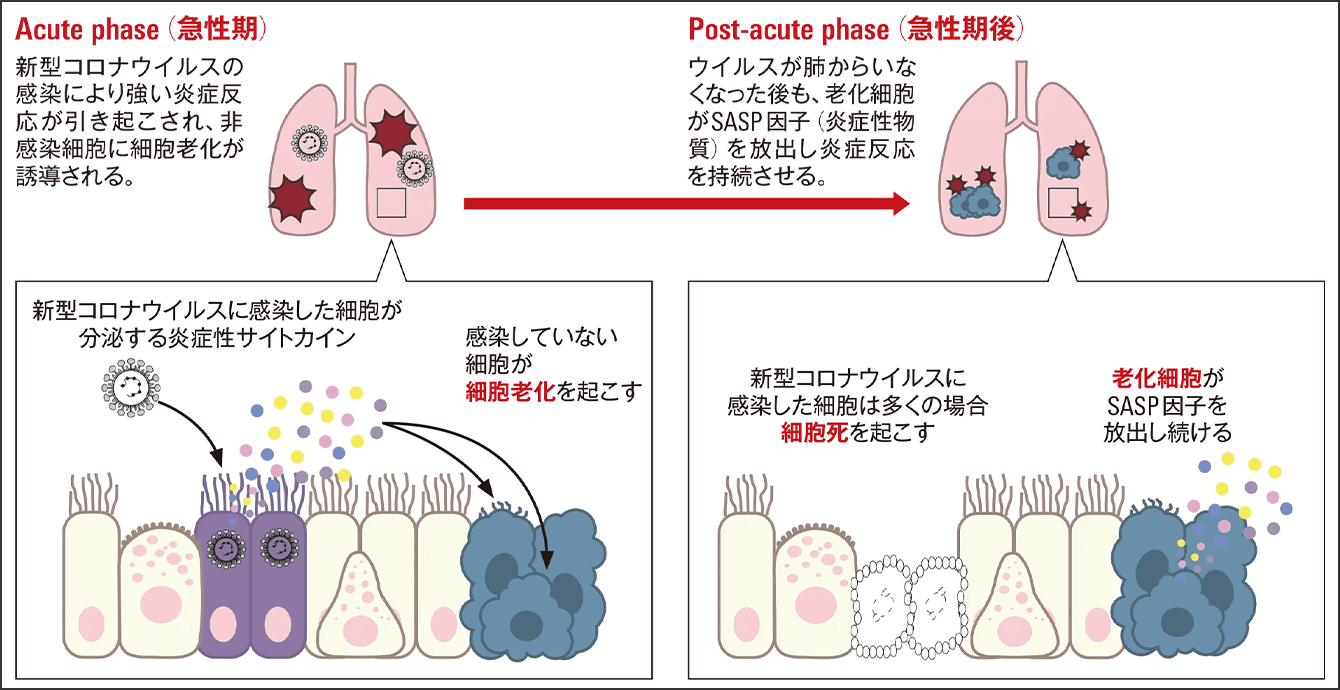
「我々の研究から、新型コロナウイルスがいなくなった後も、この老化細胞は生き残り、長期にわたり炎症性物質を放出し続けることがわかりました(図)。
 (大阪大学微生物病研究所ウェブサイトから改変)
(大阪大学微生物病研究所ウェブサイトから改変)
図 新型コロナウイルスに感染した細胞が分泌する炎症性サイトカインによる非感染細胞の細胞老化誘導新型コロナウイルスの感染によって間接的に誘導される老化細胞の存在が、ウイルスが肺から消失した後でも炎症反応が続く原因の一つになり、後遺症に関わっている可能性が考えられている。
このことが後遺症に関わっているのではないかと考えています。COVID-19の後遺症の多くに慢性炎症との関与が指摘されています。炎症が持続すると、倦怠感が続いたり、また、嗅覚異常にも影響しているのかもしれません」
老化細胞がSASPを起こすことによって炎症が持続しているのであれば、老化細胞を標的にして除去することができれば、後遺症が治る可能性も考えられるという。
老化細胞を除去する薬はセノリティックドラッグと呼ばれ、世界中で開発が急がれているが、実際に薬事承認された薬は今のところまだない。
これらのセノリティックドラッグは、肝硬変や腎疾患、がんなどの加齢性疾患に効果があるのではないかと研究されてきた。
一方で、新型コロナウイルスに感染した後の、老化細胞除去にも有効であるかもしれないという期待も持たれている。
原教授たちの研究グループが、新型コロナウイルスに感染したマウスに老化細胞除去薬を投与したところ、老化細胞が減少して、さらには炎症反応も低下したという。これにより、COVID-19の後遺症に老化細胞除去薬が有効だといえるのだろうか。
「確かに、短期間に集中的に投薬することで、炎症反応を起こす老化細胞を除去して、慢性炎症を鎮静化させることができる可能性はあります。一方で、後遺症のすべてが細胞老化によるものではないことも間違いありません」
原教授らの研究によると、ハムスターやマウスなどの実験動物では、新型コロナウイルス感染後に現れる老化細胞は、特に肺に多く存在しているという。後遺症には脳の問題や脱毛などさまざまな事柄が報告されているが、それらすべてが老化細胞だけで説明されるわけではないという。
さらに、原教授がしっかりと考えなければならないと強調するのは、老化細胞は悪い面だけではない、良い面もあるということだ。
「実は老化細胞には、傷の修復や組織構造の維持、がんの抑制など良い面もあります。炎症性物質を出す老化細胞もあるけれども、出していない老化細胞もあり、それは不規則に存在します。さらに、SASPに含まれる炎症性物質自体も悪いことだけではなく、免疫細胞を活性化させたり、周囲の細胞に増殖を促進するなど正の役割も担っている。また、良くも悪くもなく、何も物質は出さないけれども、組織の構造上、そこにいてくれることが重要な老化細胞も存在するのです」
フランスの研究グループは、肝臓の血管内皮の組織構造を維持するための老化細胞が存在し、それを除去することで、血管がボロボロになり、肝機能も低下、マウスの寿命はかえって短くなってしまったという研究結果を発表した。
つまり、老化細胞を除去することは健康寿命を延ばすことにつながるのではないかと期待されてきたが、場合によってはかえって寿命が縮んでしまうことが明らかになった。
「細胞老化は、もともとはがん抑制機構ですから、がんなど体に危険な細胞の増殖を止めるために存在しています。確かに、その一部の細胞が炎症性サイトカインを出して慢性炎症を引き起こすこともある。
ただ、老化細胞がわざわざ炎症やがん、動脈硬化を引き起こしたりするために、そういう物質を出しているとは考えにくい。なぜそういうことをしているかというと、おそらくDNAに傷がついたときに、さまざまな増殖因子やサイトカインを出すことによって、免疫を活性化させると同時に周囲の細胞の増殖を促進し、傷を修復させるような作用があるのではないかと思います。
若い人にも老化細胞はあり、その場合はがん抑制や傷の修復など体を守る働きのほうが強いともいえるでしょう。一方で高齢者になると老化細胞は負の面が強くなっていきます」
原教授たちの研究グループは、新型コロナウイルスにおいて細胞老化が免疫活性化につながるかどうかを調べる研究を行った。
ハムスターに新型コロナウイルスを感染させると、2週間もすればウイルスはいなくなって細胞老化が起きる。そのときに、このハムスターにインフルエンザウイルスを感染させる。
その結果、新型コロナウイルスに感染していないハムスターはインフルエンザウイルスに感染して体重が落ちるが、新型コロナウイルスに感染したことがあるハムスターはインフルエンザウイルスに感染せず体重もまったく減らなかったという。
「つまり、一度新型コロナウイルスに感染しておくと、(少なくとも短期的には)他のウイルスの感染が抑制される可能性があるということです。新型コロナウイルスに感染したことによって現れる老化細胞が出すSASP因子のサイトカインが、別のウイルスの感染から守ってくれているのかもしれません。だから、やみくもにセノリティックドラッグで老化細胞を除去すると、他のウイルスに感染しやすくなったり、体にとって良くないことが起きないとも限りません」
老化細胞は一様ではなく、多様性があるのだと原教授は言う。だが、現在開発が進んでいる一般的なセノリティックドラッグでは、その老化細胞が良いものか悪いものかを区別できないという。
「ですから、老化細胞を除去するのであれば、ピンポイントに短期間やるしかないと私は考えています。例えば、抗がん剤投与後に一部のがん細胞が細胞老化を起こして、生き残ることがあります。そのような老化細胞を標的にして、セノリティックドラッグを短期間集中的に投与することにより、がん細胞を除去して抗がん剤の治療効果を高めようという研究を進めています」
通常の老化細胞には、良い面も考えられるために、除去すべきかどうかについては、慎重な議論やより深い研究が必要だと原教授は言う。一方で、がん細胞が老化細胞となったものを除去することは合理的だと話す。正常細胞には、生体の恒常性を保とうとする機能がある。他方、がん細胞は、炎症性サイトカインによってがん細胞の増殖を促進している。それゆえに、老化細胞を除去することによって、がん細胞の増殖をある程度減弱できるのではないかと考え、研究を進めているという。
現在は抗老化という観点からも大きな注目を集める老化細胞だが、原教授が細胞老化の研究を始めたのは大学院生の頃、およそ30年前のことであった。
「なぜ細胞は増えなくなるのだろうという疑問から出発しました。おそらくはがん抑制のためではないかと考えて研究を始めたのですが、当時はそんなものは単なる細胞培養のアーティファクト(人為産物)だという意見が多く、研究費もあまりつかずに、注目している人も少なかった」
そんな中で、がん抑制遺伝子が細胞老化に関与していることが明らかになり、風向きが変わってきたという。
「今や細胞老化が重要だと世界的なブームになっています。老化細胞を除去すれば加齢に伴う疾患が治るという考えにはある程度期待はしていますが、慎重になる必要もあるでしょう。確かに、老化現象の一部に細胞老化が関係していることは間違いないと思いますが、それはおそらくほんの一部であってすべてではないでしょう」
原教授らは2013年、科学誌Natureに、肥満に伴って腸内細菌が変化することで、肝がんの発症が促進されることを発見したと発表した。
さらに、肥満になると腸内細菌が変わって細胞老化を引き起こすメカニズムも原教授らは突き止めた。
「大腸がんの患者さんと健常人の糞便を調べてみると、大腸がんの患者さんに特異的に増えている菌が12種類見つかり、その中の2つの菌には細胞老化を引き起こす作用があることがわかりました」
この菌を、遺伝子変異を加え大腸がんを起こしやすくしたマウスに与えると、大腸がんの発症率が高くなったという。
「細胞老化を引き起こすような腸内細菌が、一部の人では年を取ると増えてくることが明らかになりました。老化細胞は短期的にはがんを抑制しますが、老化細胞による炎症が持続することによって、がんの発症率が高くなることがわかってきました。年を取ってもこういう菌が増えないようにすれば、大腸がんの発症を抑制できるのではないかと考えています。現在、細胞老化を引き起こすこれらの菌が増えるメカニズムの研究を続けています」
がんなどさまざまな疾患に関わる老化細胞だが、翻って、COVID-19の後遺症に対しては結局どうすればいいのだろうか。
「後遺症についてはまだわからないことが多くて、どれだけ続くかもまだわかっていません。今言えるのは、ハムスターでは45日までは炎症反応が見られるということです。ハムスターは3年くらいしか生きませんから、相当長いといえるでしょう。
炎症反応からすれば老化細胞が残っていることは悪いように思いますが、これを本当に0にしたほうがいいのかどうかは、いまだにわかりません。でも100%言えるのは感染しないに越したことはないということです」
老化細胞を一律に除去することについては、原教授は慎重な態度をとる。
一方で、COVID-19の後遺症に老化細胞が関わっていることがわかったからこそ、見えてきた知見もあるという。
「もし新型コロナウイルスに感染したとしても体の中で感染拡大が起こらないようにし、サイトカインストームを起こさないようにするのが大事だと思います。感染したとしても体内で感染拡大が起こらなければ、細胞老化も起きないし、後遺症にもつながらないかもしれません。
ワクチンにはそのような効果が期待されますので、まずはワクチンを接種することが重要だと考えます。しかしワクチンだけでは防げないケースもみられますので、体内での感染拡大を防ぐ効果的な薬の開発を目指した研究も現在進めているところです」