大動脈解離は死に至ることの多い深刻な病気だ。血管の内膜に亀裂が入ると、そこから流れ込んだ血液によって中膜が剝がれるように裂けて膨らみ、大動脈内に2つの血流ができてしまうことから「解離」と呼ばれている。動脈硬化や高血圧などが関与すると考えられているが、はっきりとは分かっていない。前触れなく発症し、さまざまな臓器に障害をもたらす合併症を引き起こすが、通報・救急搬送・病院・心臓血管外科の連携プレーがスムーズにいけば助かるケースが増えている。
突然襲ってくる致死的「血管病」 生命にかかわる大動脈解離は救急医療の連携がカギとなる
構成/渡辺由子 イラストレーション/青木宣人
私たちの体は、心臓の拍動(収縮運動)によって、左心室から酸素を豊富に含んだ血液が体の隅々に送り届けられ、生命が維持されています。その通り道が、人体で最も太い血管(直径20~30㎜)である大動脈で、心臓から上のほう(頭部)へ伸び、弓状に曲がりながら心臓の後ろ側に回り、背骨の左横を下半身のほうへ向かいます(図1)。
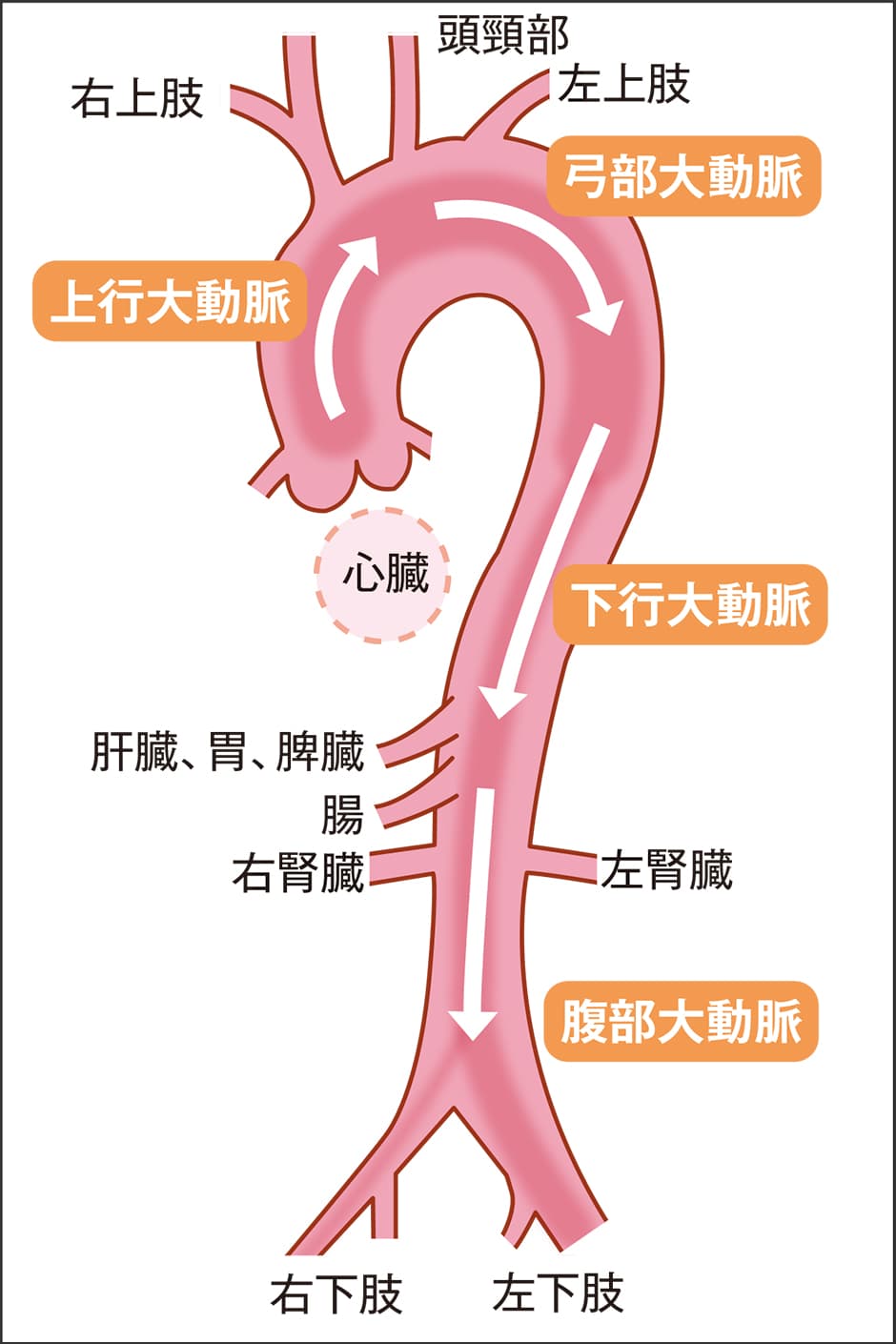
図1 大動脈と主な動脈大動脈は心臓から出ると、上行大動脈から弓部大動脈、下行大動脈、腹部大動脈へと名前を変え、枝のように分かれた動脈から重要な臓器に血液を送り届ける。
上へ向かう部分を「上行大動脈」、弓状の部分を「弓部大動脈」、下へ向かう部分を「下行大動脈」、これら3つの動脈を総称して「胸部大動脈」と呼びます。下行大動脈は横隔膜を通過して、「腹部大動脈」と名前が変わります。大動脈は、心臓に血液を送る冠動脈をはじめ、さまざまな重要な臓器へつながる血管へと細かく枝分かれして、体の隅々まで血液を運んでいるのです。
大動脈は、「内膜」「中膜」「外膜」の3層構造になっています(図2)。血液と接する内膜は薄いスベスベの膜で、その周りを柔らかく弾力性のある分厚い中膜が覆い、左心室の拍動を伝えながら、血液を体の隅々まで送り届ける原動力になっています。その外側を外膜という強い膜が覆い、動脈の構造を保っています。
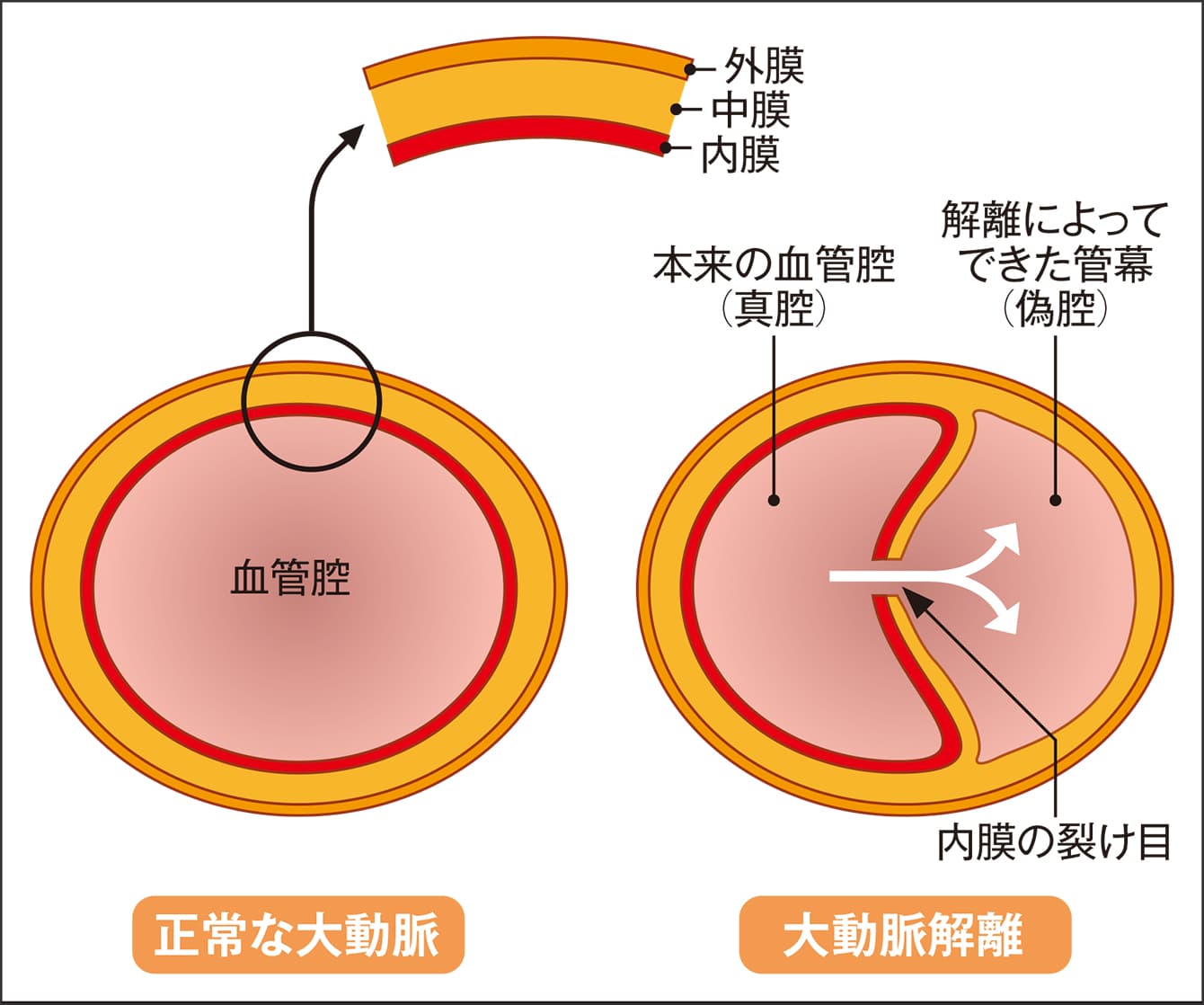
図2 大動脈の構造正常な大動脈(左)は、内膜・中膜・外膜の3層構造となっている。何らかの原因で内膜に亀裂が入り(右)、血液が中膜の中へ流れ込み偽腔を形成しているのが大動脈解離で、重要な動脈に影響が及ぶ。
大動脈内に2つの血液の通り道ができる
大動脈解離は、内膜に何らかの原因で亀裂が入り、そこから血液が流れ込むことにより、中膜が剥がれるように裂けて膨らみ、大動脈内に2つの血液の通り道ができるのが特徴です。大動脈が剥がれるようにして裂ける状態であることから、「解離」と呼ばれます。
中膜の中に血液が流れ込んだ部分を「偽腔」、もともと血液が流れていた内膜に囲まれた部分を「真腔」と呼びます。偽腔は内膜の亀裂から、心臓より遠いほうへと広がりますが、偽腔が大きくなって真腔が狭くなると、行き場を失った血液が偽腔の中を逆向きに心臓に近いほうへ進んだり、偽腔が広がって真腔に戻るように別の内膜の亀裂ができたりすることがあります。
また、亀裂が中膜で止まらずに外膜まで及ぶと、大動脈の外に出血して大動脈破裂となり、直ちに生命に関わります。さらに、大動脈自体や大動脈から枝分かれする各臓器への血管が偽腔によってふさがれ、血流が障害されると、心筋梗塞、脳梗塞、腸管虚血、腎不全、下肢動脈閉塞などの臓器虚血(臓器への血流が悪くなることで酸素が行き届かず、機能が障害されたり、壊死に陥ること)を起こすことがあり、これらの病気を想定して検査を開始したところ、大動脈解離が発見されることもあります。
大動脈解離の原因は、動脈硬化、高血圧、喫煙、ストレス、高脂血症、糖尿病、睡眠時無呼吸症候群などが関与すると考えられていますが、はっきりとは分かりません。そのため、誰に、いつ発症するかを予測するのは、非常に困難です。国立循環器病研究センターが発表した、2016年1月から2020年4月までの急性大動脈解離の発症年齢のデータでは、40代から増え、60歳以上、特に70代での発症が最も多いことが分かります。これは社会の高齢化が進むことによる高齢患者の増加が一因と考えます。また、全身の器官や組織の結合を支える結合組織が弱くなる遺伝性の疾患の「マルファン症候群」や、類似した遺伝性疾患があると、若い人でも発症する確率が高くなります。
なぜ内膜に亀裂が入るのかについては、解明されていませんが、おそらく、心臓から出てすぐの上行大動脈は、左心室から送り出される血液の高い圧を受けていること、弓部大動脈は分岐する3本の動脈が緩く固定され、全体としては曲がった構造になっていることなどにより、亀裂が入りやすいのではないかと考えられています。
大動脈解離の症状は、何の前触れもなく、背中や腰、腹部などの激痛を伴って起こるといわれていますが、一方で、血流障害によって臓器の働きに影響が及ぶと、さまざまな症状が現れることもあります。心筋梗塞による胸痛、脳梗塞による意識障害や麻痺がみられることもあります。上半身や下半身に至る動脈の血流障害で、手や足が急に痛くなり、大動脈解離が分かることもあります。
他に、解離して薄くなった壁からにじみ出るように出血する場合があります。にじみ出た血液が心臓の周りの袋である心嚢の中にたまると、心臓が十分に広がらず、全身から心臓に戻ってきた血液が心臓に流れ込まなくなり、結果として心臓から出ていく血液が減り、急激な血圧低下や意識を消失するショック状態に陥る「心タンポナーデ」になることもあります。
大動脈解離は、発症後に迅速に大動脈解離と診断され、治療の行える専門病院に搬送されることにより、救命率を上げることができるようになりました。
診断は主にCTによる画像診断で行われますが、エコー(超音波)検査で解離の起きている部位や臓器の血流障害などを確認し、治療方針を決定することもあります。
大動脈解離の治療は、解離の起きた部位によって異なります。大動脈解離の治療方針の決定に用いられるスタンフォード分類で、上行大動脈に解離がある場合を「A型」、下行大動脈から腹部大動脈にかけて解離がある場合を「B型」と分けています(図3)。A型では心タンポナーデを起こしたり、冠動脈や頸動脈といった重要な動脈に解離が及んで生命に直結する場合があり、開胸して行う緊急手術が原則です。
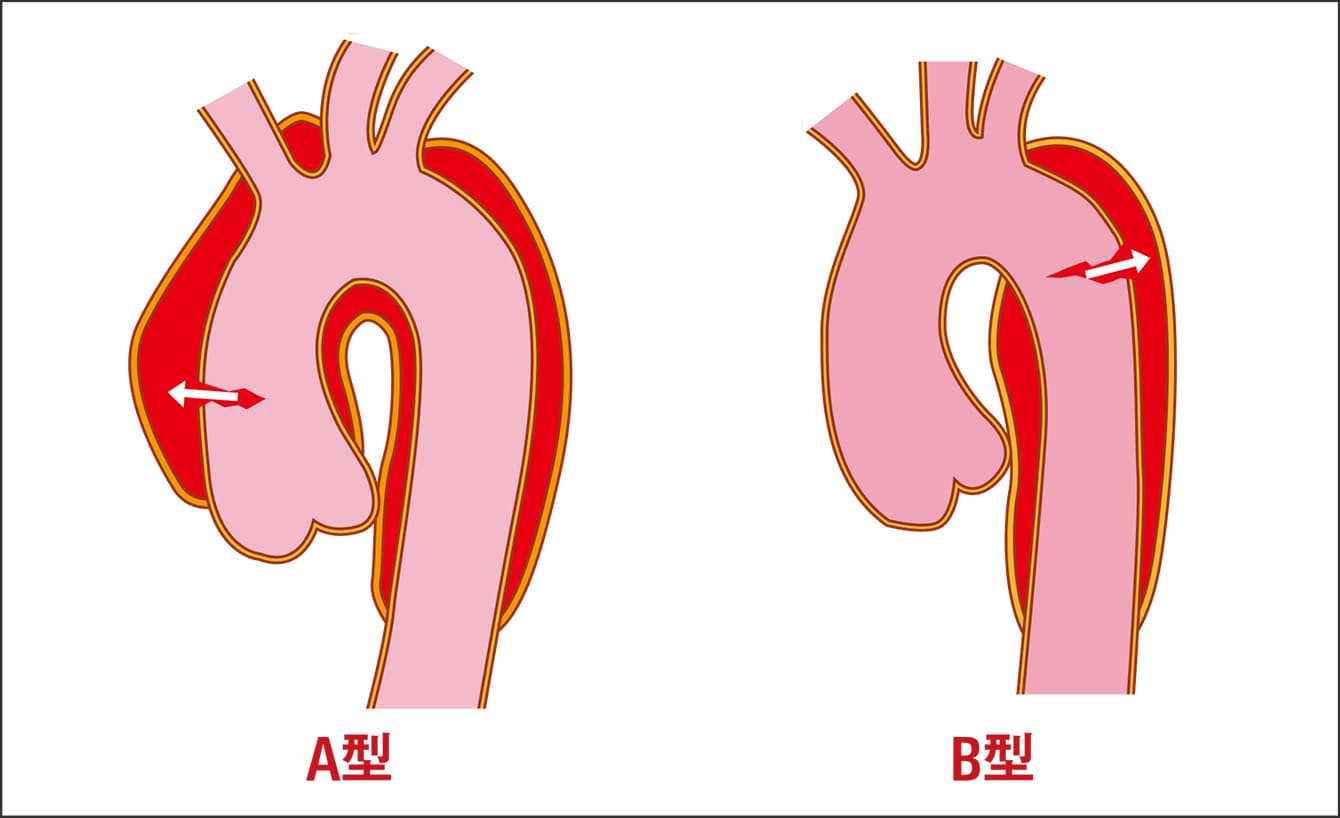
図3 大動脈解離の分類大動脈解離は、大きく分けて上行大動脈に解離が及ぶA型と、下行大動脈から腹部大動脈にかけて解離のあるB型に分類される。
B型では、血圧を下げて、激痛を和らげる治療をまず開始し、痛みが和らいでCTで大動脈の拡大がなく、安定した状態であると判断できれば、厳重な血圧管理を行います。B型でも、血流障害による臓器虚血を来していたり、破裂やショック状態、CTで大動脈の急速な拡大が判明すると、A型と同様の緊急手術が必要です。
A型ではショック状態でなくても、できるだけ早く、発症後数時間以内に手術を開始し、B型でも、臓器の虚血に対してはすぐに手術となり、救命のための手術が分単位、時間単位で行われています。A型では、救命のための緊急手術を行わないと、1時間に1~2%ずつ死亡率が上昇し、発症後48時間以内に約50%の方が亡くなるとされています。
大動脈解離を発症してから2週間までを「急性期」、2週間から3カ月間までを「亜急性期」、3カ月間以降を「慢性期」としています。急性期に適切な緊急手術や内科的治療を受けることが最も大切ですが、急性期を乗り越えた後に、解離して薄くなった大動脈の壁が次第に膨らんで大きくなっていく「解離性大動脈瘤」になると、手術が必要な場合があります。
手術は3種類
大動脈解離の手術は、救命のみを目的とした最小限度の手術しか行えない場合もありますが、解離の原因となった内膜の亀裂を取り除くか、閉鎖することが最も重要で、大きく分けて次の3つの方法があります。
①人工血管置換術(図4)
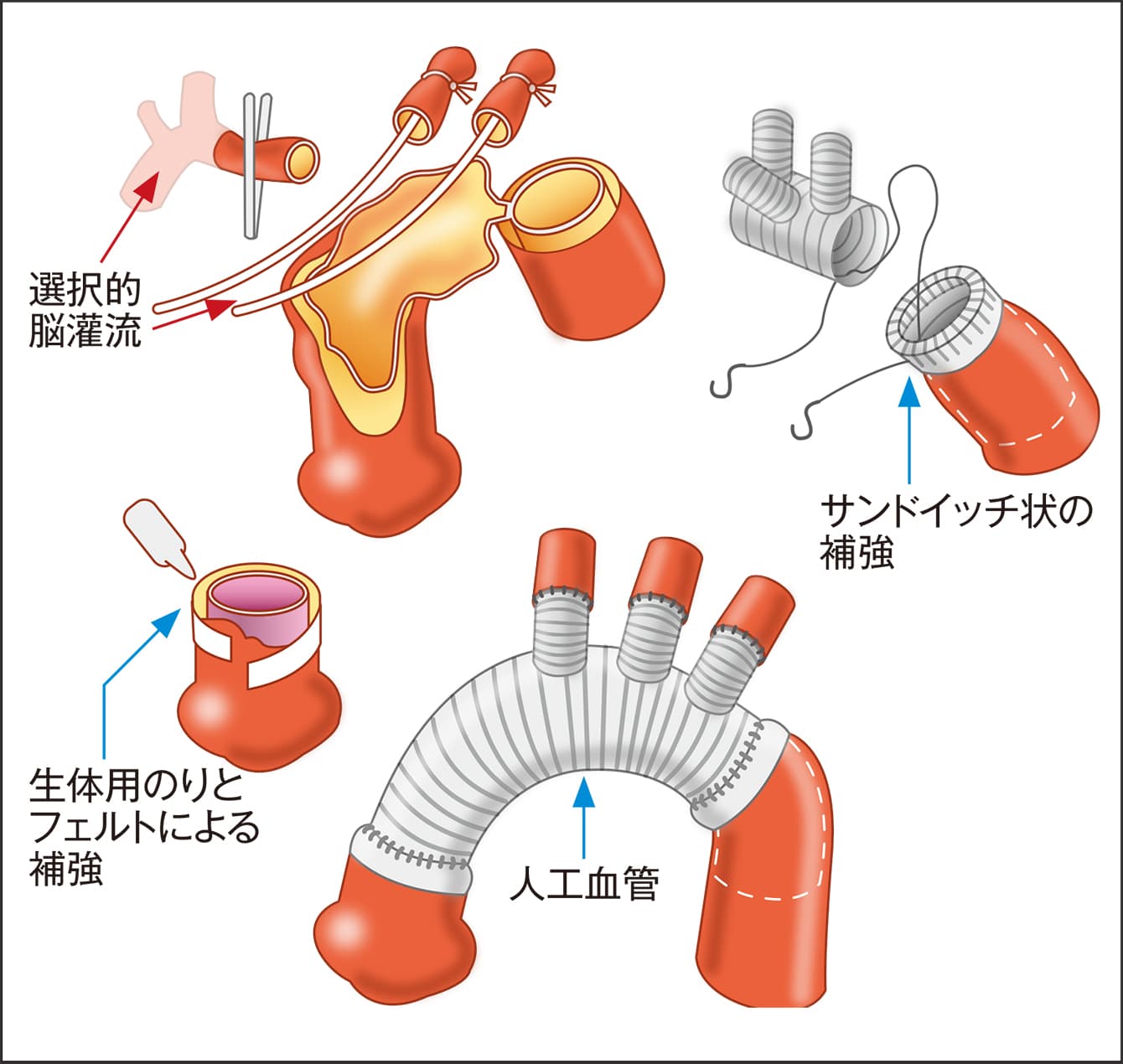
図4 人工血管置換術水道管交換の水道工事に例えられる、人工血管置換術。道路を深く掘り、水道管のバルブを閉めて断水してから水道管を交換するように、開胸や開腹し、血液の流れを一時的に止め、内臓や筋肉へのダメージを防ぎ、体を冷やしたり、脳以外への血流を停止したりする。
従来、行われている手術方法で、A型大動脈解離では、上行大動脈から弓部大動脈のすべて、もしくは一部を人工血管に置き換えます。人工心肺装置を使い、患者の血液循環と酸素供給を維持しておいて、体温を25℃から28℃に冷やしてから(低体温法)、脳以外への血流を一時的に停止する選択的脳灌流を行った上で実施します。上行大動脈から弓部大動脈を切除し、解離している大動脈をフェルトと人工血管でサンドイッチのように縫い合わせたり、生体用のりを塗って固めたりして補強し、人工血管と縫い合わせます。解離が心臓の近くまで進んでいるときは、冠動脈や大動脈弁も一緒に作り直す、基部置換を行います。最近は、将来の下行大動脈の拡大を防ぎやすくするために、人工血管置換術と同時に下行大動脈の中に、後述するステントグラフトを入れておく手術が増えています。B型大動脈解離では、下行大動脈を人工血管に置き換えます。
人工血管はポリエステル(ダクロン)製で、十分な耐久性があります。直径20~28㎜くらいの人工血管に、直径8~11㎜の枝分かれした血管が付いている人工血管もあります。人工血管置換術は長い歴史があり、手術後の経過や起こり得る合併症などのデータの蓄積があります。体への負担は小さくありませんが、改良が進み、安全性の高い治療になっています。
②ステントグラフト内挿術(図5)
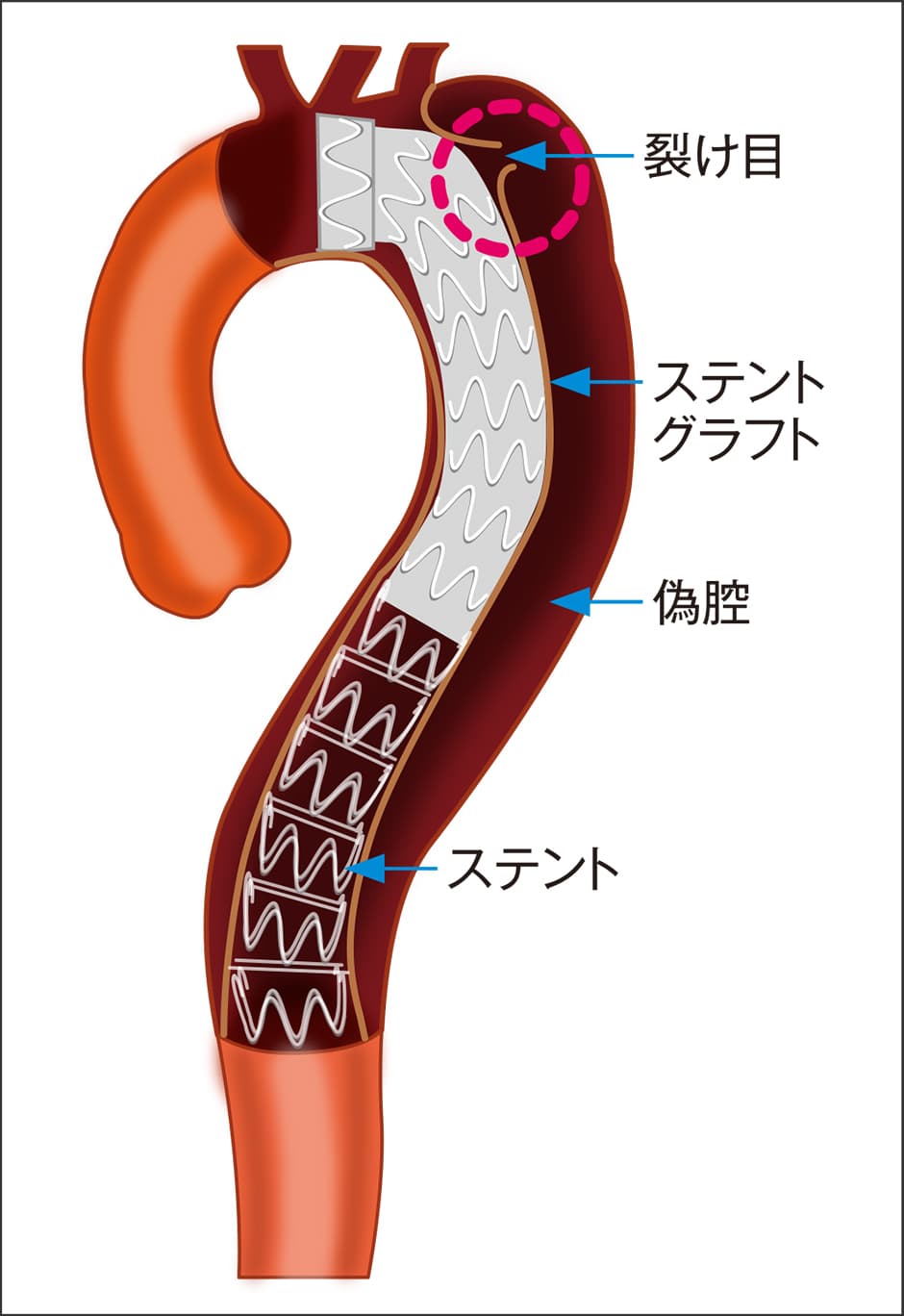
図5 ステントグラフト内挿術急性B型大動脈解離では、開胸しないため体への負担が軽い血管内治療のステントグラフト内挿術が広まっている。解離の原因となった内膜の亀裂がステントグラフトで覆われるため、血液は偽腔に流れ込むことがなくなる。
解離の原因となった内膜の亀裂を、ステントグラフトで閉鎖する治療が広まり、体への負担が人工血管置換術に比べて小さいことから、高齢者や比較的若い方でも開胸手術の危険性が高いと思われる患者への治療に選択されています。
ステントグラフトは、ステントという金属のバネを取り付けた人工血管で、ステントグラフトが収納されている直径6~9㎜のカテーテルを、脚の付け根(鼠径部)の小さな切開部位から挿入し、大腿動脈を経由して大動脈の真腔内へ進み、解離している部位で展開します。バネの力と血圧によってステントグラフトが広がって真腔内に固定されると、内膜の亀裂が覆われ、心臓から流れてきた血液はステントグラフトの中を通って先に流れ、偽腔に流れ込むことがなくなります。
ただし、この術式はすべての患者に行えるのではなく、内膜の亀裂の場所や解離の広がり具合によってはできない場合があります。ステントグラフトを確実にセットするには、大動脈の太さ、長さ、位置、曲がり具合など、多くの状況に合わせなければなりません。そのため、急性A型大動脈解離のほとんどの患者は、この術式での治療はできませんが、一方で、急性B型大動脈解離で緊急手術を要する場合には、ほとんどの患者をステントグラフト内挿術で治療できるようになり、治療成績も上がってきました。
予防的にステントグラフトを使う
慢性期の解離性大動脈瘤をステントグラフトで治療することも試みられていますが、必ずしも第1選択となるわけではなく、症状や全身状態とステントグラフト内挿術で治療できるかどうかのバランスを考えて選択されています。なお、ステントグラフト内挿術は、日本ステントグラフト実施基準管理委員会で認定された指導医か実施医が、認定された施設で行っています。
③予防的なステントグラフト内挿術
前述した2つの手術は、急性大動脈解離のために生命に関わる状態となっている場合や、解離性大動脈瘤が拡大して破裂の危険性が迫っている場合に行われますが、解離性大動脈瘤になる前に、予防的にステントグラフト内挿術を勧める場合があります。
B型大動脈解離の急性期を内科的治療で乗り越えた後や、急性A型大動脈解離の手術後に下行大動脈に解離が残っているような場合に、あらかじめ下行大動脈にステントグラフトをセットして、内膜の亀裂を覆うことで、慢性期に大動脈瘤に進むのを予防するのが目的です。大動脈の大きさや解離の広がり具合、偽腔の血流の状態などを慎重に検討して、効果が期待できる患者に実施されています。
近年、大動脈解離の患者数が増加傾向です。社会の高齢化に伴う高齢患者の増加や、医療技術の進歩により、早期に診断されて、救命率が上がったことも、増加の一因と考えられています。さらに、患者・患者家族からの救急車要請、救急搬送中の対応、病院の救急部、心臓血管外科の連携プレーがスムーズにいけば、確実に助かるケースが増えています。
当センターでは、心臓血管外科部門で3チーム体制を構築し、24時間365日、いつでも緊急手術に対応できる環境を整備しています。近隣の消防署の救急隊に対しても、大動脈解離が疑われる場合、迅速に手術を開始できるよう、たとえその後の検査で大動脈解離でないと分かったとしてもかまわないので、直ちに当センターへ搬送することを取り決めています。病院にたどり着く前に死亡してしまうケースもありますが、たどり着くことができたときは、全力で治療を行い、救命率の向上に取り組んでいます。
大動脈解離は、解明されていないことが大変多いのですが、誰にでも起こり得る病気であることは分かっており、そのように認識することが大切だと考えます。