脳と腸が影響し合う、いわゆる脳腸相関における腸内細菌が果たす役割は多様だ。中でも過剰なストレス応答の抑制は、「良い睡眠」を得るための重要な要素となる。腸内細菌の環境が良好な状態で保たれることで自律神経である交感神経と副交感神経のバランスが整い、リラックスする。寝つきが良く、深く眠れ、目覚めもすっきり——と、質の良い睡眠を獲得することができ、疲労回復にもつながる。今後の研究により、詳細なメカニズムが解明されるに違いない。
ストレスと睡眠 腸内細菌の良好な環境が自律神経のバランスを整える
構成/渡辺由子
ヒトに有益な効果を与える、生きた微生物である「プロバイオティクス」は、ヨーグルトなどの発酵食品に含まれており、古くから私たちの生活に密接に関わっています。プロバイオティクスの整腸作用はよく知られたことですが、近年の研究で新たな作用が明らかになっています。その一つが、「脳腸相関」を介したプロバイオティクスの中枢への作用です。
脳腸相関で重要な働きをする腸内細菌
ヒトをはじめ哺乳類の中枢神経系(脳)は、原始的な動物の腸管神経系が進化したものとみられています。一方で、発生学的には、腸管神経系は、胎児期に頸部の迷走神経堤細胞が腸管に沿って遊送することで形成されます。このように、脳と腸管神経系には密接な関わりがあります。
近年の研究では、腸内細菌叢の宿主の行動パターンや精神症状への作用が数多く報告されるようになり、「腸内細菌-腸-脳相関」の概念が広く認知されるようになってきました。脳から腸へ情報が伝達されるだけでなく、腸の情報が迷走神経や血液を介して脳に伝わって脳機能にも影響を及ぼすなど、脳腸相関において腸内細菌は重要な働きをしています。
腸内細菌-腸-脳相関の情報伝達経路には、大きく分けて神経因子と、液性因子の2つが知られています。神経因子は、腸管上皮細胞や消化管ホルモンを分泌する腸管内分泌細胞、腸管免疫で重要な役割を果たすM細胞や樹状細胞などが腸内環境を認識し、腸管神経叢、迷走神経を刺激することで、中枢に伝達される経路を担っています。中枢に伝えられた情報は、脳の視床で情報が統合され、適切な反応刺激が自律神経遠心路を介して、腸管および全身に伝えられます。
液性因子である消化管ホルモンや腸内細菌により産生される代謝物は、血流を通して、中枢神経系に直接的あるいは、間接的に作用します。これらの調整因子により、腸内細菌-腸-脳相関のネットワークが形成されて、ヒトの恒常性維持に大きな役割を果たしていると考えられています(図1)。
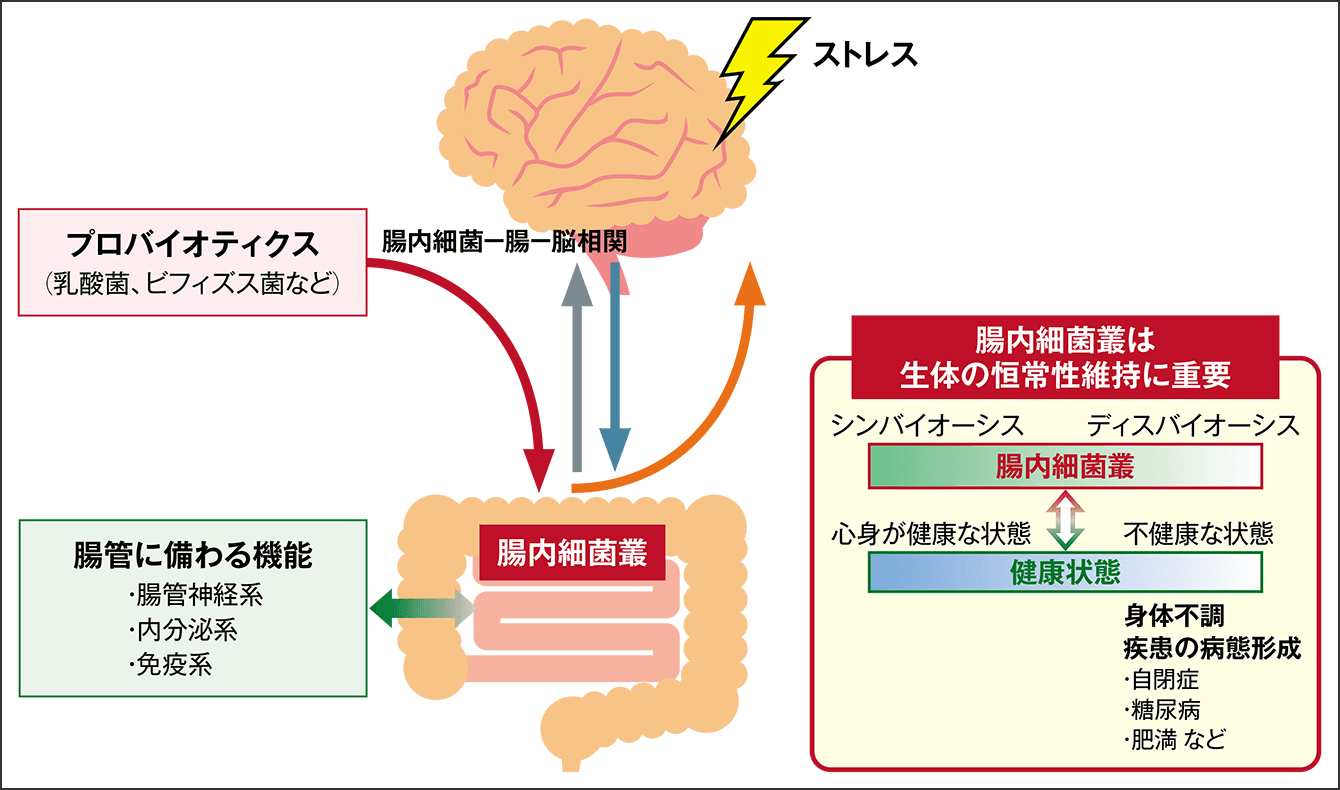
図1 プロバイオティクスのストレス緩和作用腸内に生息する腸内細菌叢は、多様性を保っている状態(シンバイオーシス)と、多様性が失われた状態(ディスバイオーシス)により、生体の恒常性維持に大きな影響を与えると考えられている。睡眠においても、「腸内細菌叢-腸-脳相関」が鍵となる。
九州大学の須藤信行教授らの研究グループは、腸内細菌をまったく持たない無菌マウスは、通常の腸内細菌を持つマウスに比べて、生体のストレス応答が過剰になることを明らかにしています。同時にプロバイオティクスであるビフィズス菌を無菌マウスに与えると、過剰なストレス応答が通常マウスと同等レベルまで抑制されることを突き止めています。
さらに、腸内細菌が迷走神経を整えている、という研究報告が出ており、非常に興味深く見ています。迷走神経は、脳と腸の情報交換経路の要であり、情報伝達量の約90%は腸から脳への情報伝達で占められているとされ、腸内細菌により調整される腸内環境の重要性が推察されます。ヒトの健康に大きな影響を与える腸内細菌-腸-脳相関について、国内外で研究が進んでいます。
「有害菌」の増殖も抑制
ストレスそのものは悪いものではなく、ある程度のストレスは生きていくうえで必要です。私たちの体には、適切なストレス応答によって、ストレスから心身を守る仕組みがある一方で、過剰なストレスが持続的にかかると、心身にさまざまな症状が現れてしまいます。私は、徳島大学のストレス制御医学教室で、ヒトのストレス状態を反映するストレスバイオマーカー(生物指標化合物)を探索する研究を続けてきました。その中で、プロバイオティクスによるストレスの軽減について、ヒトへの介入研究をスタートさせました。
この研究は3年間にわたり、本学医学部の学生延べ140人に対して、4年生から5年生に進級する際に実施される学術試験の8週間前から試験直後まで、プロバイオティクスである「L.カゼイ・シロタ株」を含有する飲料摂取群(以下、L.カゼイ・シロタ株飲料摂取群)と、プラセボ飲料摂取群とに分けて実施した、二重盲検プラセボ対照平行群間比較試験です。
- * L.カゼイ・シロタ株:2020年4月以降はL.パラカゼイ・シロタ株と分類されています。
その結果、L.カゼイ・シロタ株飲料摂取群では、ストレスに伴う身体症状(下痢や腹痛、風邪など)の出現が抑制されていました。また、ストレスがかかると分泌量が増える、唾液に含まれる副腎皮質ホルモンのコルチゾールの上昇が、L.カゼイ・シロタ株飲料摂取群では抑制されていました。
同様の変化のパターンを示したのが、血液中に分泌されるストレスホルモンなどに曝露された白血球で、どのような遺伝子が活性化されているかを調べた結果でした。L.カゼイ・シロタ株飲料摂取群では、ストレス応答遺伝子の変動が抑えられていました。腸内細菌叢の解析も行い、一般的に「有害菌」とされるバクテロイデス科の細菌の増殖が抑制されて、腸内細菌の多様性が保持されていることも明らかになりました。
3年に及ぶヒト介入研究の結果から、生体の反応として、プロバイオティクスによる強いストレス下における過剰なストレス応答の抑制、つまりストレス緩和作用があることを確信しました。これは、良い腸内環境を維持することで、ストレスへの反応の程度が調整されたのではないかと考えています。
次にプロバイオティクスの新しい機能として、ストレスを伴う睡眠をターゲットにし、2年間にわたるヒト介入研究を行いました。先の研究と同様の手法で、本学医学部生の進級時に受ける学術試験前後の睡眠の状況について、被験者94人をL.カゼイ・シロタ株飲料摂取群(48人)と、プラセボ飲料摂取群(46人)とに分け、試験前8週間から試験後3週間まで毎日飲用してもらい、調査しました。
睡眠の評価は、主観的指標に「OSA睡眠調査票MA版」という起床時に16の質問に答えるアンケートを採用し、客観的指標には自宅で簡易睡眠脳波計を使用して脳波を測定してもらいました。
睡眠の質的な改善が認められる3項目
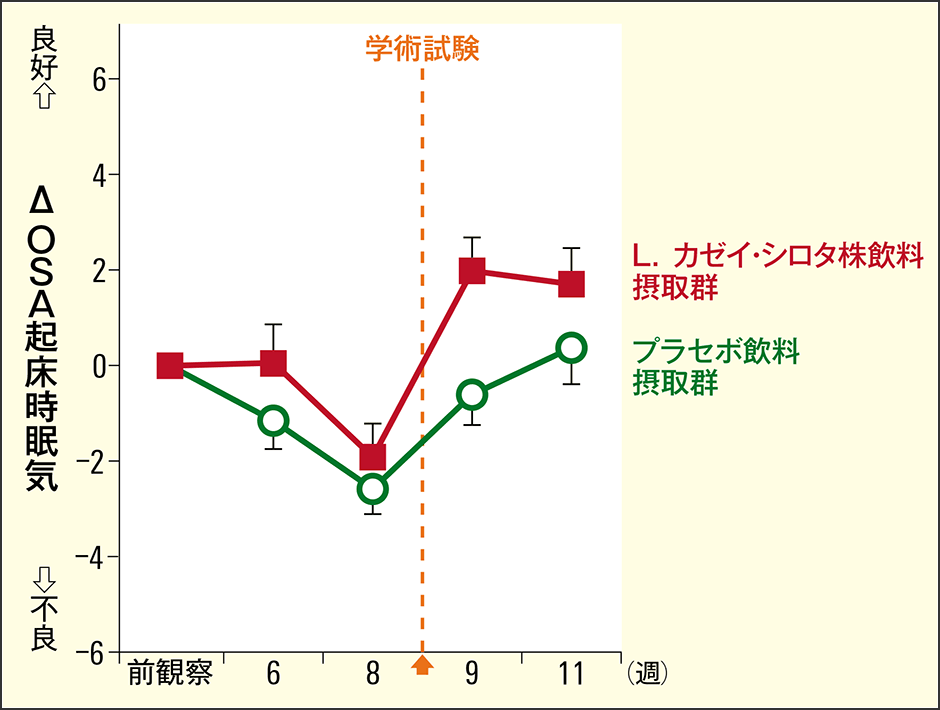
誰しも、試験が近づくにつれて不安が大きくなり、眠ったとしても熟睡した感覚が低く、起きたときに眠気を感じた経験があると思います。OSA睡眠調査票MA版の解析から、L.カゼイ・シロタ株飲料摂取群では、起床時にすっきりした目覚めを示すスコアが有意に改善されており(図2)、体感としてよく眠れたことを示す睡眠時間の延長も認められました(図3)。
 Takada M, et al. Benef Microbes. 8: 153–162, 2017.
Takada M, et al. Benef Microbes. 8: 153–162, 2017.
図2 起床時の眠気主観的指標に採用したアンケートから、L.カゼイ・シロタ株飲料摂取群では、起床時にすっきりとした目覚めが得られていると分かった。
 Takada M, et al. Benef Microbes. 8: 153–162, 2017.
Takada M, et al. Benef Microbes. 8: 153–162, 2017.
図3 体感の睡眠時間図2と同様のアンケートから、「よく眠れた=十分な睡眠時間が得られた」と体感できていることが分かった。
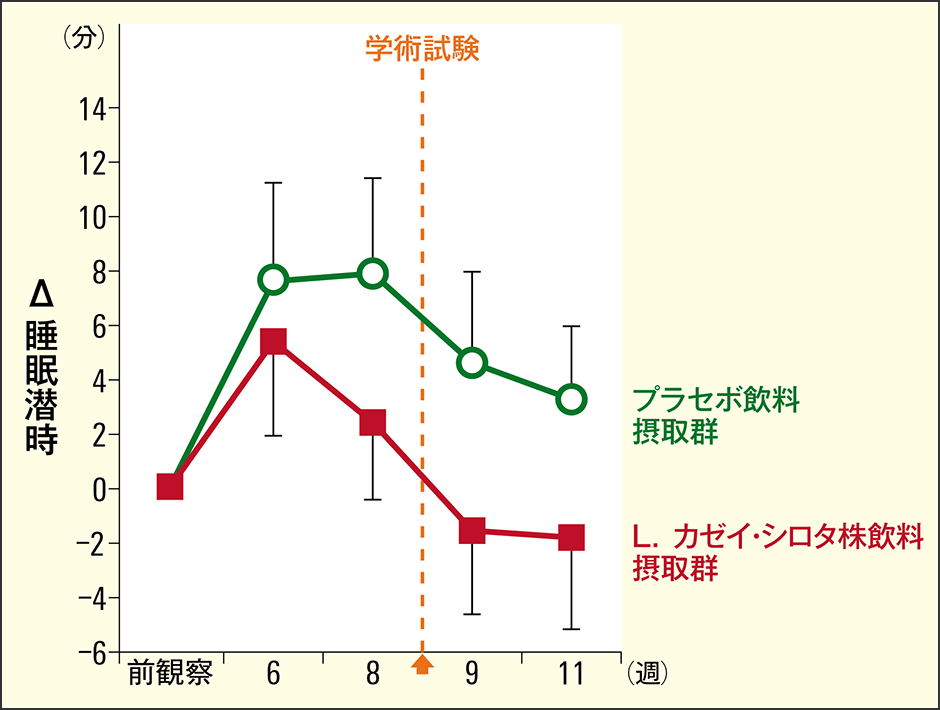
さらに、客観的指標の簡易睡眠脳波計による実測データでは、3つの項目で睡眠の質的な改善が認められました。1つ目は「睡眠潜時」で、覚醒している状態から眠りに入るまでの時間のことで、寝つきの良い悪いを表します。ここでは、L.カゼイ・シロタ株飲料摂取群では、睡眠潜時が延長するのを抑制している結果となり、寝つきの悪化を防ぎました(図4)。
 Takada M, et al. Benef Microbes. 8: 153–162, 2017.
Takada M, et al. Benef Microbes. 8: 153–162, 2017.
図4 睡眠潜時試験前の不安感により眠りにつくまでに時間がかかる傾向だが、L.カゼイ・シロタ株飲料摂取群では、寝つきの悪化を防いでいた。
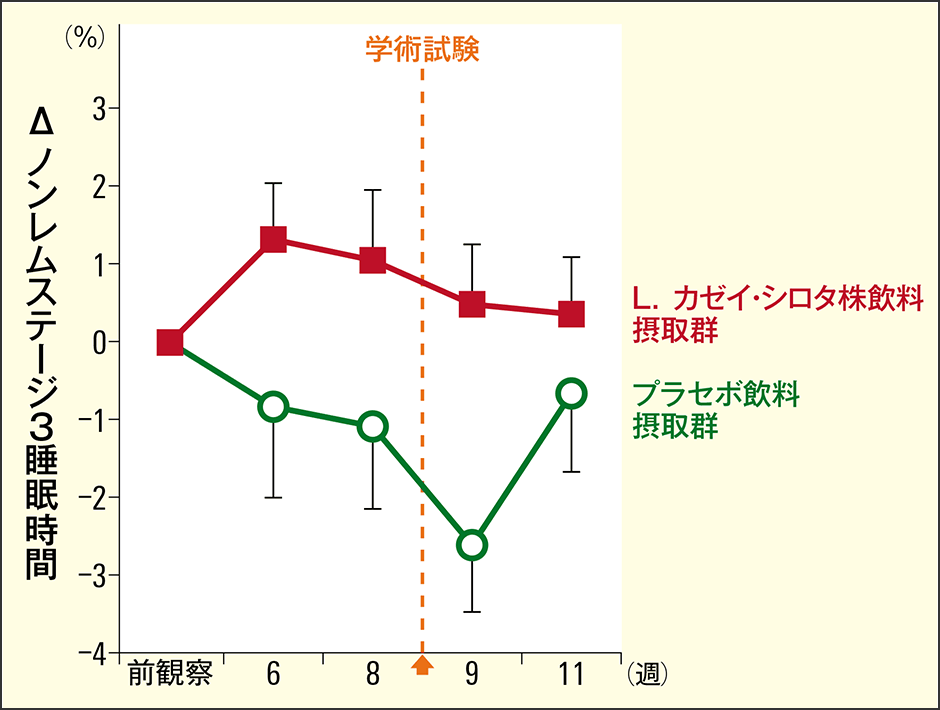
2つ目は「深睡眠時間」。睡眠は浅い眠りのレム睡眠(REM sleep)と、深い眠りのノンレム睡眠(non-REM sleep)で構成され、ノンレム睡眠からレム睡眠へと移行するサイクルを約90分で繰り返しています。レム睡眠は、眠っているときにまぶたの裏で眼球が素早く左右に動く(急速眼球運動:Rapid Eye Movement)から名づけられており、脳は覚醒状態に近く、全身の筋肉が弛緩しており、体を休ませつつ、脳で記憶の定着などが行われているとされています。ノンレム睡眠は、脳を冷却してしっかりと休ませるための深い睡眠で、ステージ1(N1)から最も深いステージ3(N3)の3段階に分けられます。今回は、睡眠サイクルの第1周期に注目して解析しました。L.カゼイ・シロタ株飲料摂取群では、学術試験が近づくにつれて、N3の深睡眠時間が短縮するのを防ぎ、試験というストレスがあってもぐっすりと眠れていることを確認しました(図5)。
 Takada M, et al. Benef Microbes. 8: 153–162, 2017.
Takada M, et al. Benef Microbes. 8: 153–162, 2017.
図5 睡眠時間深い眠りを示すノンレムステージ3について、L.カゼイ・シロタ株飲料摂取群はプラセボ飲料摂取群より、深く眠れていたと示された。
3つ目は「デルタパワー」です。脳波は、アルファ波、ベータ波、シータ波、デルタ波に分けられ、デルタ波は波長が長く、徐派(スローウェーブ)とも呼ばれています。デルタ波は、睡眠サイクルでは第1周期のノンレム睡眠のN3で頻繁に出現し、深い睡眠によって、脳の休息と回復が進んでいることを表していると考えられます。
デルタ波の量はデルタパワーと呼ばれて、深く眠れる力を表しており、睡眠の質を評価するのに活用されています。心身の疲れに対して、回復させようとする生体のポジティブな反応がデルタパワーに表れています。L.カゼイ・シロタ株飲料摂取群では、デルタパワーの値が増大し、学術試験前の勉強で脳をフル回転させたときほど、力強く深く眠れることによって脳が休息・回復できていることが示されました(図6)。
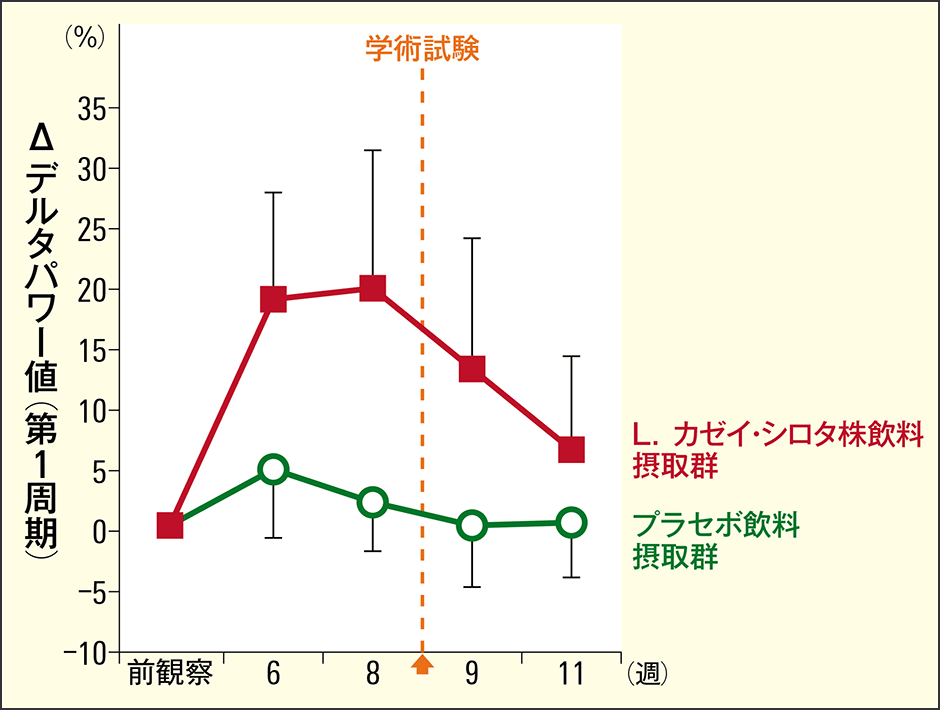 Takada M, et al. Benef Microbes. 8: 153–162, 2017.
Takada M, et al. Benef Microbes. 8: 153–162, 2017.
図6 デルタパワーL.カゼイ・シロタ株飲料摂取群は、プラセボ飲料摂取群より深く眠って脳の休息と回復が図られていることが、実験により示された。
これら3項目の改善を示した結果は、主観的指標で明らかになった、起床時の眠気の改善と体感の睡眠時間の延長と関連する客観的データと考えられます。以上のことから、プラセボ飲料摂取群に比べてL.カゼイ・シロタ株飲料摂取群は、学術試験に伴うストレスによって生じる、睡眠の質の悪化を予防できたと考えられます。
また、非常に興味深いのが、学術試験を終えて3週間後まで調査をしていますが、L.カゼイ・シロタ株飲料摂取群では、試験後の回復が主観的指標と客観的指標を合わせた5項目のいずれもで、良い傾向にありました。対してプラセボ飲料摂取群では、試験を終えてもなかなか元には戻っていません。試験に限らず、過剰なストレス下であっても、眠れることができれば、回復も早いのだと、改めて考えさせられました。
ストレス緩和・睡眠効果のメカニズム
なぜ、プロバイオティクスは「腸内細菌-腸-脳相関」によって、睡眠の質を改善することができるのでしょうか。私たち研究グループでは、腸内細菌による、自律神経への調整の作用が関与していると考えています。腸内細菌の環境が保たれることで、自律神経の交感神経と副交感神経のバランスが良い方向に調整され、寝つきが良くなり、深くよく眠れて、寝起きがすっきりとして、疲労回復につながるといった、良い睡眠に至る連鎖が起きると考えられます。
では、腸内細菌の環境が保たれた、多様性のある腸内細菌叢とはなんでしょうか。これは、個人差もあるために定義が難しく、特徴づけているものは何かは、いまだ分かりません。どの腸内細菌が、乳酸菌などのプロバイオティクスを認識して効いているのかも、まだ分かりません。
私たち研究グループでは、次の段階として、プロバイオティクスの自律神経への関わりを探っていきたいと考えています。どのように働いているのか、その効果はどうなのか、さまざまな観点から研究を進め、プロバイオティクスのストレスの緩和や睡眠への効果など、メカニズムの解明につなげていきたいと考えています。
















