
老化は宿命、とされているが、なんと若返ることができる生物が存在する。体長4~10㎜の小さなベニクラゲは、危機的状況に陥るとポリプと呼ばれる成長段階の若い形態に戻ることができる。若返るというのは、細胞を未分化の状態に戻してから、再び若い細胞に分化させることだ。この若返り機構に特異的に働いている遺伝子配列が解読された。ヒトへの応用はさすがに難しいが、肌の老化を遅らせることなどは可能性があるかもしれないという。
イラストレーション/北澤平祐

老化は宿命、とされているが、なんと若返ることができる生物が存在する。体長4~10㎜の小さなベニクラゲは、危機的状況に陥るとポリプと呼ばれる成長段階の若い形態に戻ることができる。若返るというのは、細胞を未分化の状態に戻してから、再び若い細胞に分化させることだ。この若返り機構に特異的に働いている遺伝子配列が解読された。ヒトへの応用はさすがに難しいが、肌の老化を遅らせることなどは可能性があるかもしれないという。
生物にとって老化は必然だと思われてきた。しかし、実はこの世界には若返る生物がいる。
トカゲやイモリのように体の一部を再生できる生き物は多く存在しているが、体が丸ごと若返る生き物はベニクラゲなど数種類のみだという。
ベニクラゲは、体長4㎜から10㎜程度の小さなクラゲであり、世界中の暖かい海に生息し、日本近海でも捕獲されている。この小さなクラゲが、もしかすると今後の老化研究の鍵を握るかもしれない。
ベニクラゲは死にそうな危機的状況になると、ポリプと呼ばれる成長段階の若い状態に戻ることができるため、「不老不死」と呼ばれることもある。ただどのように若返るかの仕組みについては、これまでほとんどわかっていなかった。
その神秘のベニクラゲのゲノム解読に、2022年12月、かずさDNA研究所とベニクラゲ再生生物学体験研究所、東京電機大学が共同で成功した。
研究代表者であるかずさDNA研究所遺伝子構造解析グループの長谷川嘉則グループ長は、ここまでたどり着くのに苦労があったと話す。
「これまでベニクラゲの遺伝子が読めなかったのは、クラゲが大変小さくて、さらに体重の90%以上が水分であるため、解析に必要なゲノムDNAが十分に取れなかったからです」
今回、解析に使ったのはロングリードと呼ばれる新しいDNA(塩基)配列解読技術である。遺伝子の全長を明らかにするためには、ショートリードでは不十分だったという。
「ゲノムの中には同じような配列がたくさんあるので、ショートリードだとひどいときには間違ったものを組み立てて不正確なゲノムを発表してしまうこともあります。ロングリードは1万塩基を連続して読むことができますが、ショートリードだとだいたい50〜300塩基しか読めません」
ただし、ロングリードは必要なDNAの量も多い。
今回使用したベニクラゲは和歌山県田辺湾で5年ほど前に採取したものだが、人工飼育はなかなか難しいとされてきた。ベニクラゲは条件が整えば何度でも若返るのにもかかわらず、ちょっとした環境の変化で死んでしまうことも多い。
「我々の共同研究者であるベニクラゲ再生生物学体験研究所の久保田信所長は、ベニクラゲを針でつついて14回若返らせることに成功したといいます。しかし、針でつついて若返らせられるのは久保田先生くらいの熟練の技がある人にしかできない。講習を受けても、私も他の人たちも誰も若返りはさせられませんでした」
そもそもベニクラゲに針を刺して若返らせることに気づいたのは、久保田所長が、日本で初めてベニクラゲの若返りを観察したときに、エビと同じ甲殻類の仲間である多数のカイアシ類が体全体に刺さっていたクラゲが団子状のポリプに戻ったからだという。
飼育が難しいベニクラゲだったが、東京電機大学の研究グループが、シャーレの中でクラゲを人工的に増やす新たな方法を開発した。
「これらは同じDNAを持つクローンです。そのゲノムを100匹ぐらいずつ抽出して、1500匹分を全部混ぜてようやく3㎍のゲノムDNAを抽出できました」
1㎍は1㎎の1000分の1である。1個体からクローン増幅させた1500匹のベニクラゲを使って、ようやく解析に必要なDNAを得ることが可能になった(図1、2)。
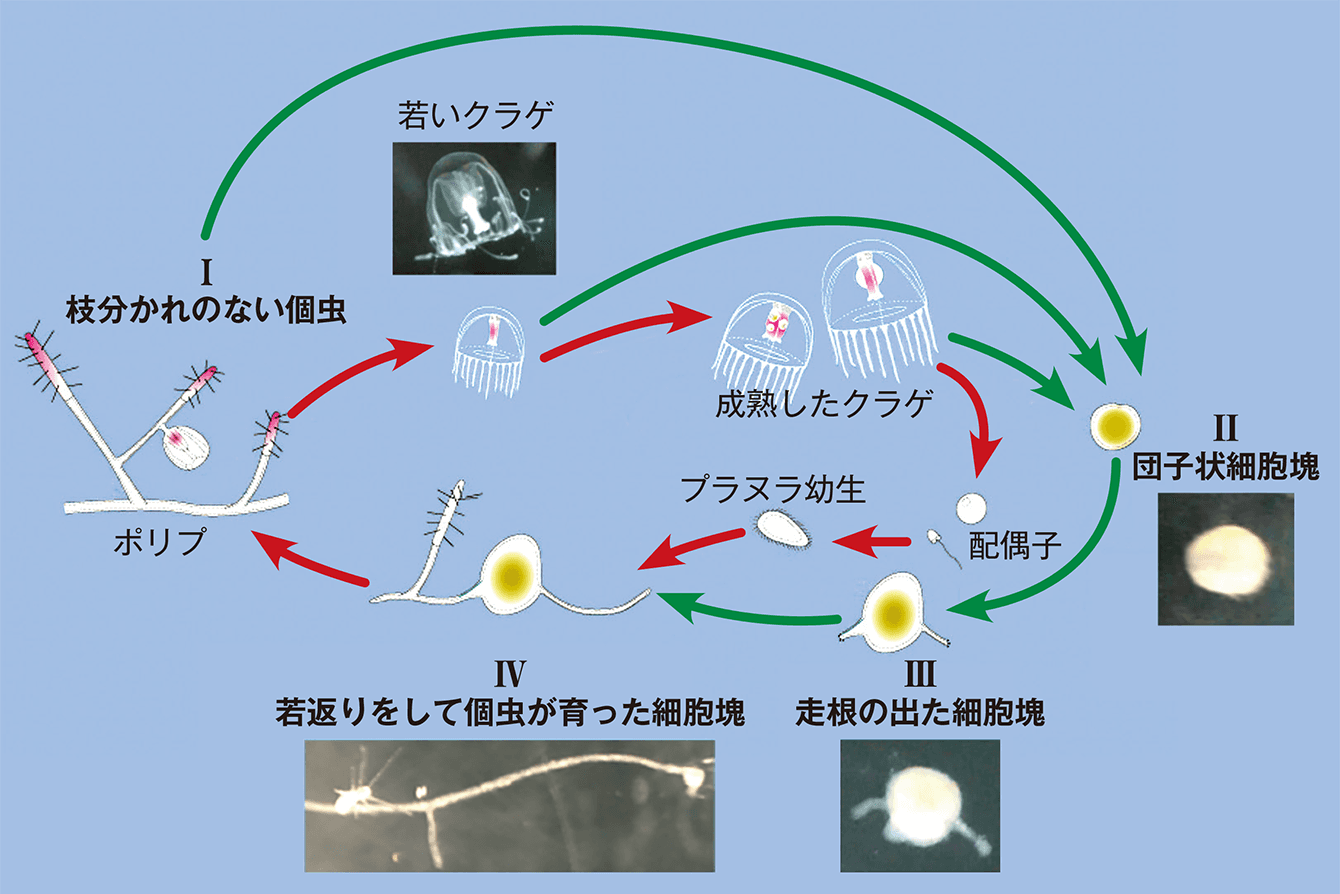
図1 ベニクラゲの生活環一般的なベニクラゲのサイクル(赤矢印)と実験室で人工的に脱分化・細分化を起こさせた場合のサイクル(Ⅰ〜Ⅳ、緑矢印)。

図2 ベニクラゲ体長4㎜から10㎜程度の大きさで、世界中の暖かい海に生息する。解析のために1500匹分のDNAが使用された。
「そこからゲノムを組み立てて、遺伝子領域を推定しました。さらに我々は独自にベニクラゲから抽出したメッセンジャーRNAを使って、実際に発現している遺伝子配列をすべて確かめました。その両方の結果から、ゲノムの大きさは約4億塩基対、遺伝子数は約2万3000個と特定しました」
前述したように成熟したクラゲからの若返りを成功させるのは容易ではない。試薬に浸けたり、刺激を与えたりすることで若返りができるという論文はこれまで存在していたが、今のところ再現性はそれほど高くないという。
そのため今回の研究では、より簡単に脱分化と再分化させることができる、ポリプから枝分かれしていない個虫の状態で切断し、解析を行った。
分化とは、多細胞生物で、特殊化していない細胞がさまざまな臓器などに形や機能が変化することを指す。脱分化は、分化した細胞が未分化の状態に変化することである。ベニクラゲの場合は、クラゲから団子状になることを脱分化、そこからもう一度若いクラゲとして生まれることを再分化という。
「ここでわかった約2万3000個の遺伝子の、他の生物との相同性を、データベースを使って調べました。それによりだいたい16%ぐらいが、ベニクラゲの特異的な遺伝子の候補だということがわかりました」
データベースに登録されている生物は海洋生物のイソギンチャクやヒドラなどクラゲに似たような生物から、ヒトやマウス、昆虫や細菌まであり、その数は遺伝子配列をタンパク質配列に変換した場合、5億1700万個あった。
現在、世界中でさまざまな生き物のゲノムを解読するプロジェクトが進行しており、かずさDNA研究所では地球バイオゲノムプロジェクトに参加して、植物を中心に解読を進めているという。
「地球バイオゲノムプロジェクトでは、150万種類のすべての真核生物のゲノムを読もうとしています。ゲノム情報が公開されている地球上の真核生物種はまだ1万種にも達していません。遺伝情報は人類の財産で、絶滅してしまったらもうその情報は手に入らなくなるのです」
この巨大なデータベースに、長谷川グループ長らのグループはベニクラゲを登録した。
ただし今回は、まだよくわかっていなかった生き物のゲノム解析ができたというだけの成果にとどまらない。長谷川グループ長は、ベニクラゲの遺伝子を解明することで、若返り機構を明らかにしようとしている。
「ベニクラゲの遺伝子の中で、他の生物と相同性のない遺伝子はだいたい16%であることはわかりました。この中で、脱分化とか再分化をするときに特異的に働いている遺伝子をピックアップしました。この期間に働いているのは、ベニクラゲの若返りに寄与する遺伝子の可能性が非常に高いと考えています」
脱分化のときには、このようなベニクラゲの特異的な遺伝子の発現が多くなったという。さらに若返りや再分化に関わっているのではないかという、もう一つの根拠がある。
「ヒトの未分化のES細胞やiPS細胞に発現するような遺伝子が、ベニクラゲの中にほとんどありませんでした。そのため、ヒトとはまったく違う遺伝子、ベニクラゲの特異的遺伝子や、違う機構でもって分化が起きているという考えに至りました」
現在、長谷川グループ長のチームは、ベニクラゲが若返る過程を調べるために、どの細胞でどの遺伝子が発現しているかを詳細に調べ、そこで、さらに若返り候補遺伝子を絞り込み、その遺伝子合成を進めているという。
「その若返り遺伝子をいろいろな生物に導入して、どのような働きをするかをこれから調べていこうと考えています。まずはクラゲに近い生物、ヒドラなどから始め、若返るかどうか調べてみたい」
若返り遺伝子は、ヒトにも応用できるものなのだろうか。
「若返りのようなものは難しいかもしれないが、例えば肌の老化を遅らせることなどは可能性があると思います」
ベニクラゲの遺伝子をヒトに発現させて、効果をみる段階にまで研究が進んだ場合、どのように遺伝子を導入するのか。遺伝子のデリバリーシステムはさまざまな研究がされているが、例えば長谷川グループ長が研究してきたヒト人工染色体もその候補になりうるかもしれないという。
「我々のグループの研究では、完全に人工の染色体、ヒトの47番目の染色体を作りました。染色体なので、今までの既存のベクターとは違い安定的です。ウイルスベクターのように、ウイルスの遺伝子がヒトの染色体に入り込んだりする可能性もありません。また染色体なので、基本的に入れられる遺伝子の長さが非常に長いことも利点です」
47番目の染色体と聞くとなんだか恐ろしい気もするが、人体には影響がないのだろうか。
「ヒトではまだ細胞でしか試していない段階ですが、マウスでは8世代200匹以上にわたって安定的に人工染色体によって遺伝子が伝わっています。人工染色体はとても小さく、相同組み換えなども起こらず、ぽつんと一人でいるイメージです」
長谷川グループ長は、ヒトの遺伝子を発現させて、 薬効をみるマウスを作ったという。世の中には病気を引き起こす遺伝子、例えばアデノシンデアミナーゼ欠損症のような治療が難しい病気がある。
しかし、正常な遺伝子を人工染色体に載せることで、難病の治療につながる可能性も模索しているのだという。
このような先端の技術も組み合わせて、ベニクラゲの若返り遺伝子をヒトに導入する日もいつか来るのだろうか。ただし、もしもベニクラゲで若返り機構がわかったところで、ヒトとは生物としてあまりに違いすぎるようにも思える。
「確かに、ベニクラゲの遺伝子がヒトやマウスでどういう作用をするかはまだわかりません。しかし逆に言うと80%ぐらいは同じ遺伝子の中で、ベニクラゲの特異的な遺伝子は協調して若返りの際に働いているわけです。ですから、これが他の遺伝子とかタンパク質になんらかの作用をしているのは間違いない。それがヒトの若返りや健康にどう役立つかはこれからの研究次第ですが、今まであるような遺伝子では考えられなかった、新しい機能を持つ可能性もあります」
ベニクラゲは面白い生物として注目はされてきたが、科学的な成果としてはしばらく大きな進捗がなかった。長谷川グループ長は47番目の染色体の研究など最先端の研究から、どうしてベニクラゲに関心を持ったのだろうか。
「ベニクラゲ再生生物学体験研究所の久保田先生と以前からカラオケ仲間で、不老不死を研究するためにぜひ協力してほしいと言われたのが最初なのですが……」
ただ、長谷川グループ長は生物学がバックグラウンドであり、生態系に興味を持っていた。
「もともと僕はカエルの方言の研究をしていました。野外でカエルが鳴いているのは雌を呼ぶためです。雌は視覚情報はほとんど使っておらず、声だけで相手を選んでいます」
そのカエルの鳴き声には方言があり、地方によってモテる雄の鳴き方にも変化があったという。
「ツチガエルという茶色いカエルは、長い鳴き声の雄がモテていました。また地域差もあり、北のほうは寒いせいか『ぎゅぎゅ』という短い鳴き声で、南に行くと『ぎゅーぎゅー』と長くなります」
別の地域のカエルの鳴き声を録音し、雌に聞かせて反応をみる実験もしたという。
「あらかじめ雌にはホルモンを打って発情させておき、自分の生息している地方と遠い地方の雄の鳴き声を流すと、自分の地方にしか行かなかったりとか、両方行くものがいたりとか、さまざまなことがわかりました」
その頃の生物学的なバックグラウンドと現在のゲノムの研究を、ベニクラゲでは組み合わせることができたという。
長谷川グループ長が今後解き明かしたいのはやはり若返りの仕組みだという。
「若返りはどのようなものか、どういう遺伝子が働いて、どうしてそういうことができるのかということを明らかにしたいです。そして、可能であればやはりヒトに役立つ研究に結びつけたいと思っています」
ベニクラゲによって不老不死も目指せるのだろうか。
「脳の記憶だけコンピュータに移してまた戻そうなどという研究もあるぐらいですから、肉体だけ若返えらせることができたら、もう本当に死なないのかもしれません」
しかし、これからさらなる高齢化社会になっていくのに、それでもヒトはやはり若返りをしたほうがいいのだろうか。
「『フランケンシュタインの誘惑』というTV番組ではないですけれど、やはり研究者は目の前にあることを解明したいものです。そしてベニクラゲの若返り機構の解明を通して、ヒトの老化や健康寿命の延伸を研究することはヒトに役立つことだと信じています」