ヒトと長く共生してきた腸内細菌は多様化、つまり共多様化する。共多様化した腸内細菌は免疫システムや健康に影響を与えているが一方で、どの種がどの程度、ヒトと共進化しているかは明らかになっていない。共進化とは、環境を共有する生物同士がお互いに影響し合って進化することで、共進化した菌はヒトの進化を知る上でも、腸内細菌の健康や疾病への関与を探る手掛かりとしても重要だという。共多様化した菌種の探索は、共進化した菌種を探す第一歩となる。
特集 腸内細菌最前線 疾病予防や治療につながる「共多様化」した菌種の探索
構成/飯塚りえ
進化の過程では、環境を共有する生物同士が影響し合うことがあります。進化生物学の用語で「共進化」といわれます。昆虫や無脊椎動物では、こうした共生システムの例がよく見られます。アブラムシは植物の蜜を吸いますが、そのままでは生存に不可欠な栄養素を吸収することはできません。そこでアブラムシの体内にいる共生細菌が蜜を分解して、アミノ酸やビタミンを供給します。この共進化の歴史は非常に長く、今ではアブラムシと菌がそれぞれ単体で生きていくことはできないほどです。そのためアブラムシの母親は、自分の遺伝子と共生細菌をセットにして次世代へ授け与えます。太古の昔に、真核生物に取り込まれた菌が、今、ヒトの中にミトコンドリアとして存在する過程に似ています。
共進化した菌はヒトの進化を知る上で重要
では、ヒトと腸内細菌は共進化してきたのでしょうか? 腸内細菌は、数百もの種がヒトの腸内にすみ、ヒトの免疫システムや健康に影響を与えています。しかし、どの種がどの程度共進化してきたのかよく分かっていません。共進化した菌はヒトの進化を知る上でも、治療ターゲットとしても重要だと考えられます。親から子へ、何世代も菌が受け継がれ、菌とヒトが環境や歴史を共有しながら多様化していく、「共多様化」した菌種を探すことは、共進化した菌種を探す出発点です。共進化と共多様化は似通った概念ですが、共進化は自然淘汰が必須な点で、共多様化と用語を分けています。私は、進化生物学の立場から、それぞれのゲノムを解読して比較し、腸内細菌とヒトの共多様化について明らかにしたいと考えています。
腸内細菌とヒトの遺伝子の関連については、乳糖にまつわる研究で明らかになっています。
共多様化した菌が、世代を通して安定して維持されるメカニズムの一つに、ヒトの遺伝子の影響があります。例えば、「乳糖不耐症」は、小腸から分泌される消化酵素「ラクターゼ」が不足しているために、乳糖を分解することができず、摂取すると下痢等の症状を起こすものです。このラクターゼを産生する遺伝子「ラクテース」の遺伝子型を見ると、腸内のビフィズス菌量を予測できることが、複数の国や研究グループで確認されています。
日本人に多い、ラクターゼが分泌されない遺伝子型を持つ場合、牛乳などを飲んで乳糖が小腸に入ってくると、乳糖がそのまま大腸に行きます。すると、大腸に乳糖がたくさんたまるので、乳糖を好むビフィズス菌が増えることになります。しかし、ヨーロッパ系の人たちはラクターゼが分泌される遺伝子型を持つ割合が多いので、乳糖が小腸で分解吸収され、大腸には乳糖が届きません。必然的に、ビフィズス菌のエサが減り、他の菌が増えてしまうのです。ここでは、ヒトと菌が糖を巡って競争関係にあることで、ヒトの遺伝子型と菌量の関係が維持されています。
逆に、協力関係の例もあります。唾液に含まれる消化酵素「アミラーゼ」は、ヒトの唾液アミラーゼ遺伝子「AMY1」によって作られます。この酵素が多ければ多いほど、唾液による炭水化物の分解が進みます。よって、アミラーゼの分泌が多い人ほど、唾液では分解されない複雑な糖が大腸に届き、アミラーゼの分泌が少ない人ほど複雑な糖だけでなく単純な糖も大腸に届きます。すると、アミラーゼの分泌が多い人ほど複雑な糖を好むルミノコッカス属の菌が増えていきます。ですから、AMY1の遺伝子型を見ると、ルミノコッカスの量を推測できることが分かっています。
狩猟採集から農業や畜産へと発達し、乳糖や炭水化物からエネルギーを得ることがヒトの生存に重要になったことが知られています。ヒトの遺伝子の進化だけでなく、それに伴う腸内細菌の進化も、ヒトの進化に貢献していることが示唆されています。近年、こうした個々の菌と遺伝子の関連がいくつか明らかになっていることからも、腸内細菌がヒトと共多様化している可能性は高いと考え、この研究に着手しました。
DNA配列を探し出すことで系統樹が可能に
私たちは、まず、アフリカ(ガボン、カメルーン)、アジア(ベトナム、韓国)、ヨーロッパ(ドイツ、英国)の6カ国から計1200人以上のヒトの唾液と糞便を集めて、それぞれのDNAを抽出しました。そこからヒトゲノムと腸内細菌のメタゲノムのデータセットを作成し、進化の歴史を表す系統樹を作り、それを比較することにしました。
ヒトゲノムや培養された細菌を用いて系統樹を作成する手法はすでに確立されていますが、あらゆる細菌が混ざったメタゲノムというDNAのシーケンスデータから個々の細菌の系統樹を作成するのは、従来、技術的に困難でした。しかし、腸内細菌への注目度が上がったこともあり、研究をスタートした2018年にはすでにさまざまなツールが開発され、個々の細菌種について、遺伝子マーカーといわれる、特有のDNA配列を探し出すことで、系統樹を作成することが可能になりました。
そうして、まずは成人に多い58種の真正細菌と1種の古細菌を対象に系統樹を作り、ヒトとの共多様性を解析したところ、アフリカ、ヨーロッパ、アジアと、それぞれの地域ごとに、ヒトの持つ菌株と相関を示す菌種が現れました(図1)。59種のうち36種に統計的に有意な共多様性が見られたのです。同時に、地域とはまったく無関係に出現している菌株もありました。この系統樹を見ると、想定していた通り、ヒトとの共多様性を示した細菌の多くは、アフリカを起源としていました。
- * 菌株:同じ細胞から分裂増殖した菌。
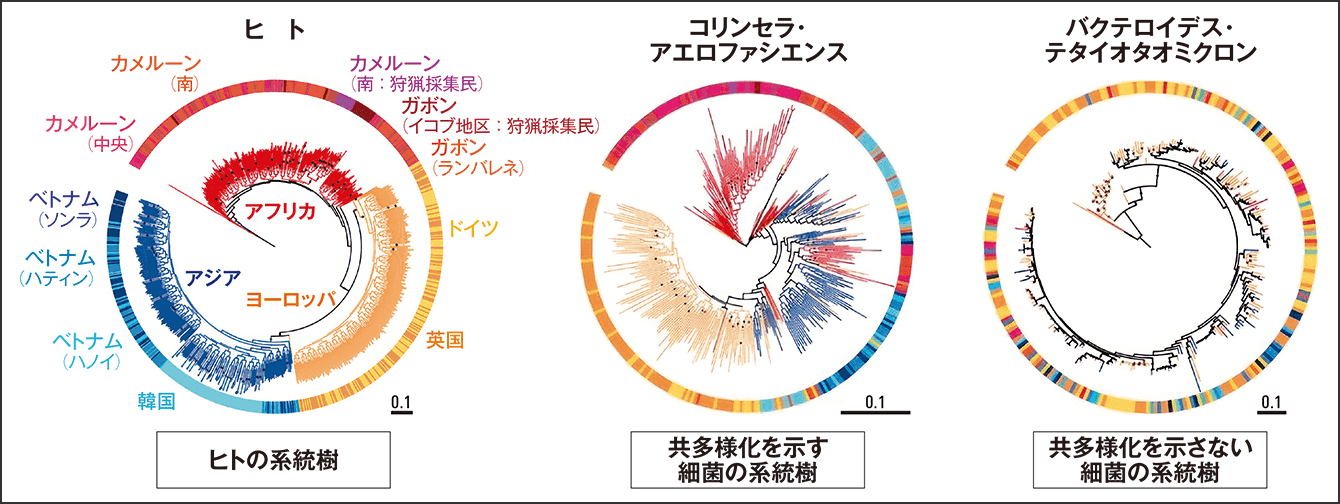
図1 ヒトと腸内細菌の共多様性ヒトの系統樹と微生物の系統樹を比較して共多様性の度合いを測定した。系統樹が一致する、つまり共多様化を示している細菌は色が一様だが、共多様化を示さない細菌は色が混ざっている。一致しない場合は集団間で腸内細菌が頻繁に行き来したことを示す。中間の相を示すものもある。
さらに、これに加えて、公開されている19カ国のヒトのメタゲノムと、27種のサル類のメタゲノム、また1000〜2000年前に北米に住んでいたヒトの糞便のメタゲノムも用いて分析したところ、前述の研究を裏付ける結論を得られました。例えば、ヒトと共多様化した細菌種では、サル類特有の菌株がヒトの菌株の祖先であることを示す系統樹が得られました。他のチームの先行研究には、ゴリラ、チンパンジー、ヒトと腸内細菌との共多様化を調べたものがあり、そこでも、霊長類と、あるビフィズス菌の種類が同じ進化をたどっていることが分かっていますが、ヒトの集団間で、腸内細菌の共多様化を示したのは本研究が初めてです。では、ヒトと共多様化している菌と、共多様化していない菌では、何が違うのでしょうか。
共多様化している菌ほどゲノムサイズが小さい
腸内環境と菌の特性を考慮すると、大変、理に適った結果が出ました(図2)。
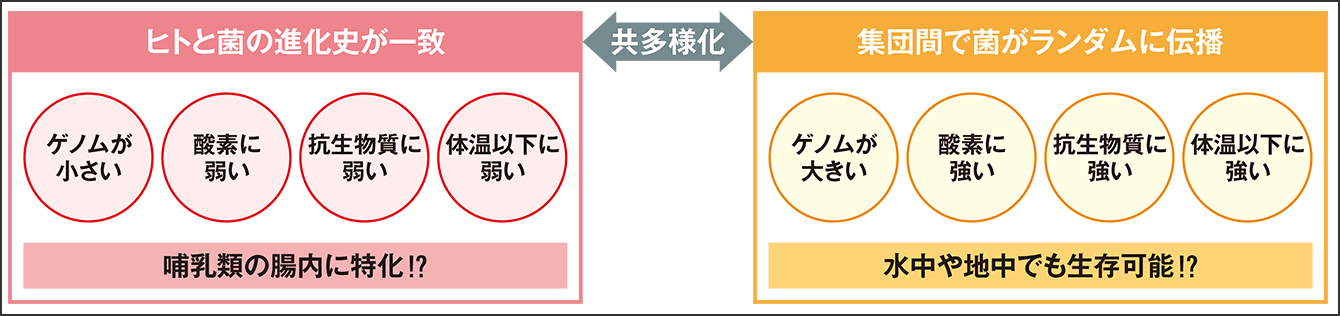
図2 ヒトとの共多様化の有無による腸内細菌の特徴ヒトの腸内という閉じた環境に適応した菌は、それにふさわしい合理的な特徴を示している。
まず、酸素が苦手な嫌気性の菌ほど集団特異的にきれいな系統樹が出ています。腸内細菌の中には、短時間なら水中でも生きられる菌や空気中でも生きられる菌がいますが、それらの系統樹には、ヒトとの共多様性を示すパターンが見られません。
もう一つは温度です。菌を、37℃と室温とで培養してみると、ヒトとの共多様性を示す菌は室温での培養の成長速度が極端に落ちる一方、共多様性の少ない菌は、室温など温度の変化にも対応できます。ヒトとの共多様性を示した菌は、腸内の安定した温度を好むのです。
3つ目に、抗生物質への耐性です。微生物はさまざまな抗生物質を産生しているので、自然環境で生きる菌はそれに対する耐性が必要です。そのため、対応する遺伝子を多く持っているのです。しかし、すみかを腸内に特化している菌は、他の菌の抗生物質への耐性を持つ必要が少なく、従って対応する遺伝子も持っていません。結果的に、抗生物質への耐性が低くなります。
腸内で共多様化している菌ほど、ゲノムサイズが小さい傾向にあることも発見しました。自然環境下の菌は多様な環境に対応するため多くの遺伝子を必要としますが、安定した腸内環境下に移りすんだ場合、それほど多くの遺伝子を必要としません。遺伝子を多く維持していると、細胞分裂が遅くなり、増殖のための遺伝子のメンテナンスに負担がかかるなど、菌にとっては進化学的なコストがかかります。そのため共生細菌は余計な遺伝子を持たずゲノムサイズが小さくなることが予測できます。冒頭の昆虫と共生細菌の例でも、共生に伴うゲノムサイズの縮小は数多く確認されており、ほぼ遺伝子を持っていない菌も存在しています。ヒトの腸内細菌もそのような共生関係の初期段階にあると考えられ、ヒトと共多様化した菌がどれだけ依存しているのかを明らかにすることが今後の研究課題です。
今、私たちのチームは、ヒトの移動に伴ってどのような菌が一緒に移動し、どのような菌は脱落したり、置換されたりするのか、それがヒトの遺伝子とどう関わり進化にどのような影響を与えたのかを解明したいと考えています(図3)。
 ©Pixeleiderdown
©Pixeleiderdown
図3 ヒトの移動と腸内細菌の伝播ヒトが大陸を移動するのに伴って、菌(菌株)も移動し、次第に共多様化していく。
例えば、胃ガンの原因ともなるヘリコバクター・ピロリ(ピロリ菌)に関して、菌の進化とヒトの疾病という観点で興味深い報告があります。
南米・コロンビアのアンデス山脈高地の町は、10万人当たり約150人と、世界的に見ても胃がんの発生率が高いことで知られています。この町に住む人はアメリカ先住民が多いのですが、胃がんとなった住民のピロリ菌株は、植民地開拓者によって持ち込まれたヨーロッパ系の菌株と置き換わっていました。他方、コロンビアの別の町の住民は、10万人当たり6人程度の発生率です。この住民の場合、自身の遺伝子も、また持っているピロリ菌の遺伝子もアフリカに起源をたどることができました。
ピロリ菌の起源はアフリカにあり、ヒトの分布とともに広がり共多様化して、ヒト集団それぞれのピロリ菌を持つようになったのですが、この研究では、自身が元々持っていたピロリ菌株であれば共生でき、起源の違うピロリ菌株ではヒトへの病原性が変わってしまうことを明らかにしています。言い換えれば、同じ菌株でもヒトの遺伝子型によって、共生できたり、不都合が生じたりする可能性があるのです。結核の原因となるマイコバクテリウム・ツベルクローシスもアフリカを起源とし、ヒトと共多様化し、病原性に関して同じような報告があります。
遺伝的ルーツや地域で菌種や菌株が異なる
私たちの研究によって、ヒトの腸内細菌も遺伝的ルーツや地域によって菌種や菌株が異なることが明らかになりました。だとすれば、ヒトと長く共生している腸内細菌においても、ピロリ菌と同じような現象があるのではないか。あるとしたら、どのように起こったのか。ヒトとの共多様化を示すのはどのような菌か、私たちはその歴史をたどりたいと考えているのです。
私が今、研究拠点としているのは、アメリカのアリゾナです。言うまでもなく、アメリカは移民の国です。さまざまな国から移住してきた人々は、それ以前に住んでいた、あるいは、生まれた国の菌株を持ってきているはずです。しかし、定住して数世代がたったときに、例えば、抗生剤の使用、食事の変化、他の菌株にさらされることによって、自身の祖先が持っていた元の菌株を失ってしまう可能性もあります。
すると、土地の移動を経て、どのような菌は残り続け、どのような菌や菌株は置換されてしまうのか、ということを調査することができます。そして世代を経てもヒトが維持している菌とヒトの遺伝子との研究を深めることで、ヒトがどのように環境に適応してきたのか、進化の過程を解き明かす一助になると考えています。
同時に、ヒトの遺伝子と共に移動する菌や菌株のミスマッチによって、突然、共進化が崩れ、その結果、影響が出てしまう形質や病気も探索できればと考えています。
先に紹介したピロリ菌の現象は、疾病の原因を解明する点からも示唆に富んでいます。アフリカ系の遺伝子を持った人ならアフリカ系の菌株は害を及ぼすことはなく、アフリカ系でない遺伝子を持った人がアフリカ系の菌株を持つとがんが誘発されるのは、つまり菌株が、宿主の何らかの遺伝子に依存しており、それがなくなると暴走してしまう例です。
腸内細菌は、免疫をはじめヒトの健康に大きく影響を与える要素ですから、こうした関係を見ていくことで、ヒトの疾病予防にもつなげることができると考えています。現代では、遺伝子とさまざまな疾病の関係が明らかになっており遺伝子検査によって個人の疾病の確率も統計的に示唆されるようになりました。ここに、遺伝子と腸内細菌の共多様化の情報を加味することで、将来の疾病予防や治療につながることが考えられます。例えば、「あなたの遺伝子型であれば、この種の、この菌株を持っているはずだが、別の地域の菌株を持っている」といった情報を、遺伝子検査とセットにし、腸内細菌が一種のバイオマーカーのような役割を果たせる可能性もあるでしょう。まずは、現代病とも呼ばれるアレルギーや喘息といった免疫との関わりが深いものについて、着手しつつあります。