大豆などから作る「代替肉」はあくまで肉の代用品だが、牛や豚などの細胞を培養して作る「培養肉」は動物由来のタンパク質で、「本物」の肉だ。いくつか生産方法はあるが、とりわけ筋肉や臓器を細胞から組み立てる再生医療の手法を用い、微生物を栄養源として大量生産を目指す研究が注目されている。目標は「いかにも“肉”といった感じ」という。おいしい培養肉ステーキが普通に食べられる日がやってくる!
特集 微生物とサステイナブル 目標は「本物」のステーキ! 再生医療技術で作る培養肉
構成/茂木登志子
人工的に作る肉には、大豆などの植物由来の「代替肉」と牛や豚などの家畜の細胞を培養して増やす「培養肉」があります。私が研究で取り組んでいるのは後者です。
培養肉の発想自体は新しいものではありません。私も研究に取り組むようになって知ったのですが、英国のウィンストン・チャーチルは、1931年にエッセイの中で「鶏の胸肉や手羽肉を食べるために丸ごと一羽育てるようなことをやめ、それぞれの部位を育てるべきだ」という趣旨のことを書いていたそうです。日本でも手塚治虫が漫画『ジャングル大帝』に人造肉を登場させています。
いずれも世に出た当時は“夢のような話”でした。夢が現実になったのは、2013年。マーストリヒト大学(オランダ)のマーク・ポスト教授が、世界で初めて牛の細胞から作った培養肉のハンバーガーを発表しました。「ティッシュエンジニアリング(Tissue Engineering:組織工学)」の技術を用いて開発したものです。しかし、140gの培養肉を作るのに25万ユーロ、つまり3000万円余りも費用がかかるというので、実用化には程遠い話でした。
その後、テクノロジーの進化とともにさまざまなコストダウン策が講じられてきました。また、日本を含めた世界中で培養肉のベンチャー企業が設立され、競うように開発が進められています。シンガポールでは、昨年、世界初の培養肉(鶏肉)販売を承認しました。今年初めに販売開始となったことも報じられています。また、日本国内でも培養フォアグラの供給が始まると聞いています。
環境に負荷をかけない食肉生産
この背景には、地球規模の理由が3つあります(図1)。1つ目は、人口増加や生活水準向上(食の多様化)による食肉需要の拡大による食料不足です。需要の増加に見合う供給量が確保できないかもしれないという「タンパク質クライシス」が懸念されています。
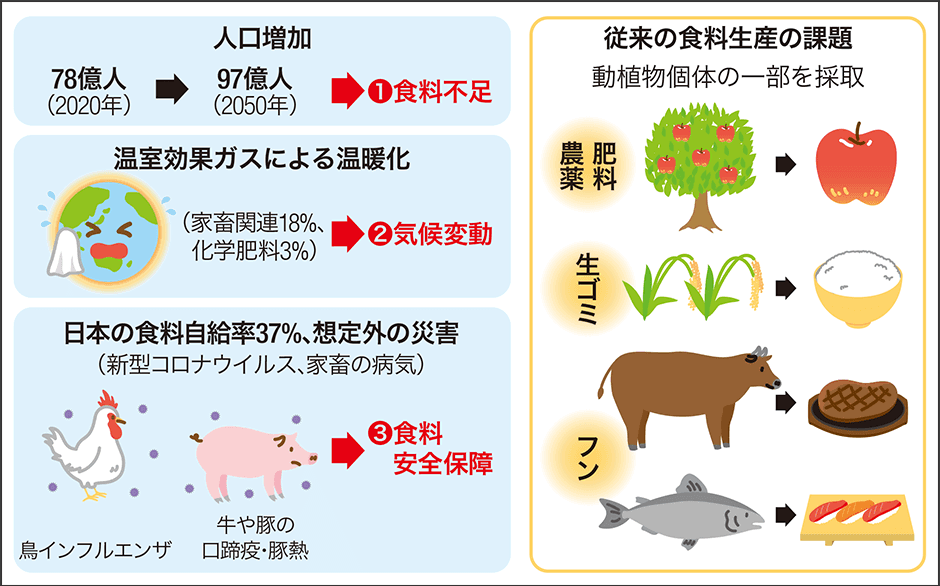
図1 培養肉開発が求められる背景人口増加による食料不足、家畜飼育関連による地球環境負荷、感染症など想定外の災害に備えた食料安全保障として、循環型食肉生産システムが求められている。(イラスト:三上里菜)
なぜかというと、食肉増産はたやすいことではないからです。食肉生産には、家畜を飼育するための土地や水、穀物飼料、糞尿処理が不可欠です。これらが環境破壊を招いたり、温室効果ガス排出によって気候変動などにつながったりすることが指摘されています。つまり、チャーチルが言うように従来のやり方ではなく、環境に負荷をかけない持続可能な食肉生産が求められているのです。これが2つ目の理由です。
3つ目は、食料安全保障です。私たちは新型コロナウイルスの感染拡大という想定外の災害に直面しています。牛や豚の「口蹄疫」、豚に広がる「豚熱」、鶏の「鳥インフルエンザ」など、家畜にもウイルス性感染症があり、これまでに何度となく流行し、その度に殺処分と消毒が行われてきました。こうした病気で家畜が飼育できなくなると、食肉は不足します。あるいはまた、人獣共通感染症などが発生すれば、家畜もヒトも健康が損なわれてしまう恐れもあります。新型コロナウイルスの感染拡大で実体験したように、想定外の災害は、いつ、どのような形で、どこで起こるかわかりません。想定外のことが起こっても、食料調達および確保を可能にすることが必要です。
では、どのようにして培養肉を作るのでしょうか。私たちは組織工学的方法による培養肉の作成方法開発に取り組んでいます。
私たちが食べている肉というのは、筋肉や脂肪などを合わせた総称です。筋肉は、筋線維が集まって束になった組織です。したがって、培養肉作製は筋肉組織を作るということになります。
簡潔に説明しましょう(図2)。研究段階では、最初に生きている家畜から筋肉組織を採取し、その「筋芽細胞」を培養します。筋芽細胞というのは筋線維の由来となる単核細胞で、この細胞が集まって相互に融合し、成熟すると、最終的に筋線維となります。ただし、形状はまだペースト状です。これを、しっかりとした歯応えのある筋肉組織に構成し、適度な脂肪その他を加え、成形すると培養肉ができあがります。
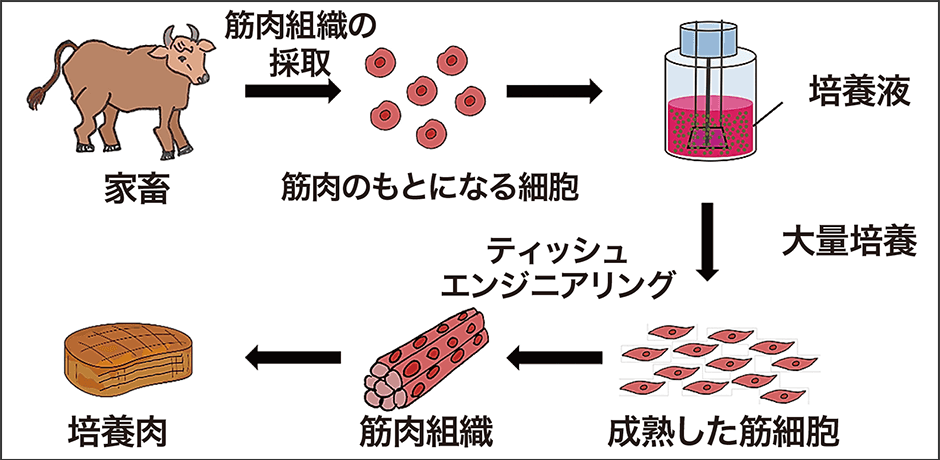
図2 培養肉の作製プロセス家畜から採取した筋肉のもとになる細胞(筋芽細胞)を栄養成分などを含む培養液で培養し、できた細胞を組織化して肉に仕上げる。
実用化にあたっては、いくつかの課題があります。主要なものは、培養液、立体構築、おいしさの3つでしょう。
藻類による循環型培養システムの構築
細胞培養液には、アミノ酸やグルコースなどの栄養成分が含まれていますが、それらは穀物由来です。研究用に使用する細胞培養液は少量ですが、培養肉が食肉生産量の何割かを占めるようになれば、大量の培養液が必要になります。コスト面と環境負荷の面から、解決すべき課題といえます。私も研究が進む中でこの問題に気づき、藻類を用いた循環型細胞培養システムの構築を模索しているところです。これについては最後にまた触れたいと思います。
課題の中でも難関なのが、筋肉組織に構成する過程です。生分解性の高分子材料を用いてあらかじめ作製した立体的で多孔性のブロック内に細胞を播種する方法や、細胞とコラーゲンなどを混和して鋳型に流し込む方法、細胞を少量のゲルと一緒に1つずつ3Dプリンターを用いて立体的に並べていく方法、細胞の集合体を剣山状の金属ニードルやメッシュ状の金属デバイスに刺すように積み重ね、組織化した後に金属デバイスを抜き去る方法などがあります。私たちは後述する細胞シートの積層化という方法で培養肉を作製しています。
最後においしさ、すなわち食感や味つけです。食感を出すために硬いものを混ぜていたり、家畜由来の脂肪やコラーゲンを加えたりしている培養肉もあるのですが、そうすると動物を犠牲にしないという本来の目的とずれてしまう。食感を出すのは、細胞を鍛えたり重層化したりすることで解決できるのではないかと予想しています。味については、エンドユーザーの嗜好に合わせて製造販売メーカーが工夫するところです。ただし、独自の肉を設計できるのですから、健康的で高栄養となるような配慮があるといいでしょう。私見ですが、噛む力が低下している高齢者には、ミンチ段階で必要な栄養素を加えておいしい味に仕上げれば、食べやすい栄養食になるのではないかと考えています。
現在までに私たちは、ウシ筋芽細胞シートの積層化により、厚さ1㎜程度の培養ハムの作製に成功しています(図3)。残念ながら、味はわかりません。なぜなら、試食することができないからです。理由は2つあります。1つ目は、食品として許可されていないこと。2つ目は、倫理上の問題です。大学の研究室で作製した培養肉を試食するにはいろいろな制約があるからです。

図3 細胞シートで作った培養ハム現時点の研究段階で完成した培養ハム。皿に添えられたプチトマトより少し大きい。(東京女子医科大学と早稲田大学の共同研究による)
私は心不全治療のための「心臓を作る」ことを目的として、1999年から再生医療の研究に取り組んできました。再生医療の中でも、細胞を材料として組織・臓器をどう組み立てていくかというところに比重を置いた研究です。なぜ、私を含めて多くの再生医療の研究者が培養肉を手がけているかというと、どちらも細胞から組織を作製するティッシュエンジニアリングを用いているからです。
細胞から組織を作製するにはいくつかの方法があります。培養肉は、細胞とその周囲を取り囲んで構造を支える細胞外マトリクスで構成されます。これまでの主な方法では、細胞外マトリクスの代替として生分解性高分子のスキャフォールド(足場)を用いていました。しかし、そこにはスキャフォールドの一部が残存したり、細胞外マトリクスを主成分とする結合組織に置換したりという、食の安全性や品質に関して解決すべき課題が残されていました。そこで私たち研究チームは、スキャフォールドを利用しないで、作製した細胞シートを積層化する方法を用いています(図4)。

図4 細胞シート法温度応答性培養皿から取り出した複数の細胞シートと藻類を交互に重ねて積層し、立体的に細胞を積み上げる。
再生医療の研究で開発した細胞シート
実は、通常の培養皿でシート状に細胞を培養しても、タンパク質によって細胞同士が結合し、培養皿に張り付いてしまいます。タンパク質を溶かして細胞シートを取り出そうとすると、細胞同士もバラバラになってしまうので、細胞シートもバラバラになってしまいます。この課題を解決するために開発したのが「温度応答性培養皿」という特殊な培養皿で、これを用いることで、温度を変化させるだけで培養皿から細胞シートを取り出すことが可能になりました。
もともとこの細胞シートは、再生医療の研究で開発したものです。すでに臨床・治験ではさまざまな用途で使用されています。2016年1月に保険適用となり、重篤な心不全治療に用いられている「ハートシート」(テルモ社)もその一例です。心臓の筋肉が薄く伸びて血液を送り出す力が弱くなった拡張型心不全の患者さんの心臓に、その患者さん自身の太ももの筋肉細胞(骨格筋芽細胞)から作った細胞シートを貼ります。すると、周囲の心臓組織の細胞を活性化させるサイトカインの効果で、血液を送り出す力が回復します。
このように再生医療において私たちは、シート状の細胞を単層あるいは積層化して組織を作製して移植するという独自の概念「細胞シート工学」を提唱し、研究開発を進めてきました。これらの成果を生かしつつ、産学連携して培養肉の研究も進めているわけです。今はまだ薄いハムレベルですが、細胞シートを少しずつ重ねていくことによって、最終的にいかにも“肉”といった感じの立体組織、つまりステーキ肉の構築を目指しています。
培養肉の作製方法で解決すべき課題の一つが、穀物由来の培養液だと述べました。この培養液をサステイナブルなものに転換しなければなりません。そこで私たちは、藻類に注目しました。
藻類は微生物ですが、微生物といえばこれまで肉のタンパク質を分解してうま味のペプチドを引き出すなどに用いられていました。それを、逆に肉を作るというボトムアップに使う発想はどこから生まれたのか。実はこれも再生医療研究からの発想です。
細胞シートを積層しても、血管網がなければ酸素や栄養が供給されないし、アンモニアなどの有害代謝産物が蓄積するので、細胞は壊死してしまいます。ところが、藻類と細胞シートをサンドイッチのように重ねて共に培養することで、厚い立体心筋組織の作製に成功しました。私たちはこの藻類と動物細胞の共生リサイクル細胞培養システムを端緒に、培養肉の作製にも藻類を用いることを着想したのです。
藻類は、光を当てるとCO2や窒素源などの無機物から、栄養素である糖分やタンパク質を産生します。そこで、穀物の代わりに藻類から、これらの栄養素を抽出・分解して培養液とすることにしました。すでに複数の藻類から動物細胞の培養に必要な基本的な栄養素であるグルコース、アミノ酸、ビタミンが抽出可能であり、それらの藻類抽出液が実際に従来の培養液の栄養素の代替となることを実験で確認しました。また、動物細胞が排出したアンモニアを、藻類がアミノ酸産生のために利用することで、培養液を浄化することも確認できました。こうした研究成果から、光エネルギーがあれば、光合成能を持つ藻類と動物細胞を循環培養することで、藻類は動物細胞に栄養素やビタミン類を提供し、動物細胞はそれらを利用して藻類に必要なアンモニアなどを産生するという、互いに必要なものを与え合う循環型の培養システムが構築できるのではないかと期待しています。現在、ムーンショット型農林水産研究開発事業「藻類と動物細胞を用いたサーキュラーセルカルチャーによるバイオエコノミカルな培養食料生産システム」というテーマで研究開発を進めているところです(図5)。
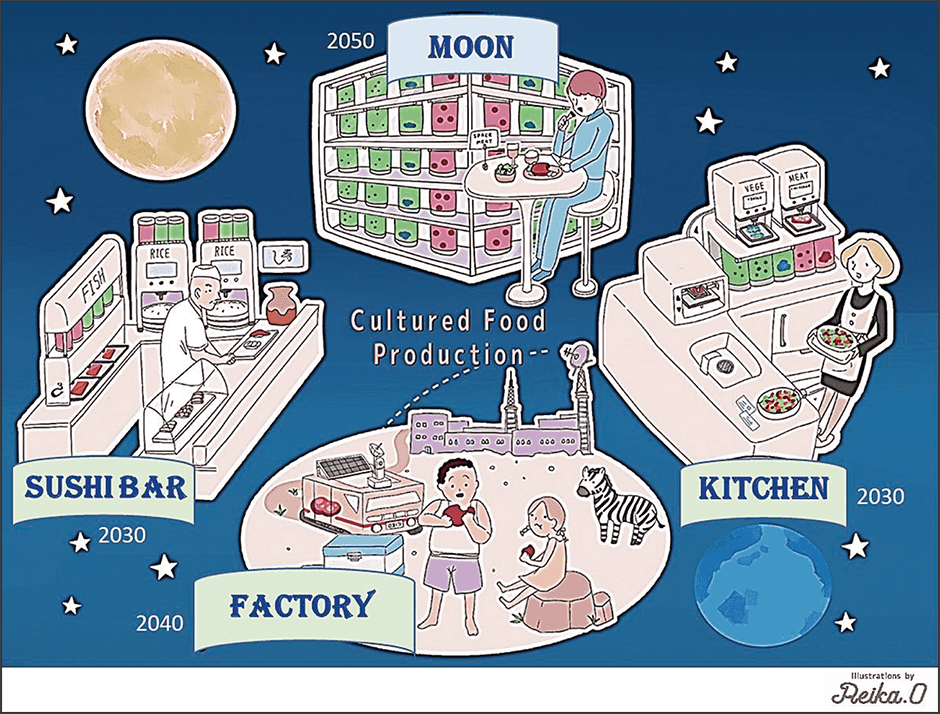
図5 循環型の培養食料(肉)生産システムの未来図これは研究チームが描く「未来図」であり、地球と宇宙で「近い将来に実現したい目標」だ。地球環境に負荷をかけない循環型システムで食料安全保障に備える。
宇宙で食料生産を目指す計画
この循環システムが構築できれば、穀物を飼料とした家畜飼育による食肉生産システムを、光エネルギーを利用して培養した藻類を栄養源とした筋芽細胞の培養と組織化による培養食肉生産システムに転換していくことが可能になります。それはまた、宇宙や南極基地などの閉ざされた環境でも食肉生産が可能になることを示しています。すでに複数の企業や大学からなる「スペースフードスフィア」が、宇宙での食料生産を目指す計画をスタートさせ、2030年代後半に月面で培養肉の生産を目指しています。私たち研究チームもこれに参画しています。
実は、循環器内科の臨床から再生医療の道に進む際、宇宙飛行士公募の情報に接して「宇宙飛行士になりたい」という夢を抱いたことがあります。そのせいか宇宙への関心をずっと持ち続けていました。研究を通して宇宙と関わることができる今は、宇宙でのサステイナブルな食肉生産システム構築の実現が、私の研究テーマであり、夢でもあります。
チャーチルの予言あるいは提言も、『ジャングル大帝』で手塚治虫が描いた人造肉も、その当時は“夢みたいな話”でした。しかし科学の進化は、これまでにいくつもの夢を実現させてきました。夢はかなうと信じています。培養肉の研究も、再生医療での「心臓を作る」という長年の夢の実現に役立つと期待しています。